صفحه 1 از 1
برخورد دو اتم هیدروژن
ارسال شده: یکشنبه ۱۴۰۲/۱/۱۳ - ۱۳:۱۹
توسط decoder
سلام
اگه دو تا اتم هیدروژن خنثی و سرد که توی حالت پایه قرار دارن به هم برخورد کنن چی میشه؟ (فرض کنید شرایط ایزوله باشه و این دو اتم با محیط بیرون برهمکنش الکترومغناطیسی نداشته باشند)
Re: برخورد دو اتم هیدروژن
ارسال شده: سهشنبه ۱۴۰۲/۱/۱۵ - ۲۰:۰۱
توسط decoder
decoder نوشته شده: ↑یکشنبه ۱۴۰۲/۱/۱۳ - ۱۳:۱۹
سلام
اگه دو تا اتم هیدروژن خنثی و سرد که توی حالت پایه قرار دارن به هم برخورد کنن چی میشه؟ (فرض کنید شرایط ایزوله باشه و این دو اتم با محیط بیرون برهمکنش الکترومغناطیسی نداشته باشند)
میخواستم ببینم اگه این دو تا اتم به هم بخورن الکترون هاشون از حالت پایه به حالت برانگیخته میرن؟؟
Re: برخورد دو اتم هیدروژن
ارسال شده: سهشنبه ۱۴۰۲/۱/۱۵ - ۲۱:۴۴
توسط MRT
انرژی جنبشی آنها به صورت امواج الکترومغناطیس تابش می کند
همانطور كه میدانیم میانگین سرعت حركت ملكولهای گاز نیتروژن در دمای اتاق و فشار یك اتمسفر 5.5 متر بر ثانیه است كه مسلما با كاهش دما ، این سرعت كاهش پیدا می كند ولی تصادم ملكولهای گاز با یكدیگر اجتناب ناپذیر است و این تصادمها ایجاد حرارت هر چند كم ولی امواج الكترومغناطیس تولید و منتشر می كند كه میتواند نامزد مناسبی برای منشاء امواج پس زمینه كیهانی نیز باشد . چرا كه توده های گاز هیدروژن و هلیم در كیهان به طور گسترده ای پراكنده شده است.

Q مقدار انرژی لازم جهت افزایش یك درجه كلوین جهت یك كیلوگرم گاز هیدروژن را نشان می دهد .
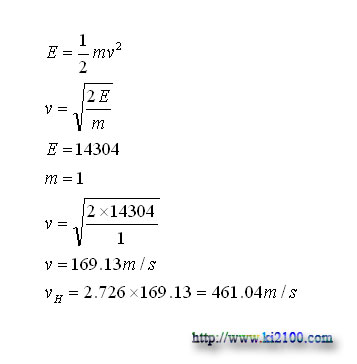
VH سرعت حركت محاسبه شده برای اتمهای هیدروژن جهت تامین این مقدار انرژی لازم است ( تبدیل انرژی جنبشی به حرارتی به علت برخورد و تصادم ) كه با در نظر گرفتن فشار پایین در فضا و شرایط محیطی منجمله فعالیت شدید ستارگان ، چرخش و حركت اجرام در فضا ، میادین الكترومغناطیسی و ... بسیار محتمل و ممكن به نظر میرسد. اینك اگر تصادم شاخ به شاخ دو اتم هیدروژن را در نظر بگیریم سرعت به 326 متر بر ثانیه كاهش پیدا می كند و اگر تصادم دو ملكول هیدروژن را در نظر بگیریم سرعت به 230.53 متر بر ثانیه كاهش پیدا خواهد کرد.
Re: برخورد دو اتم هیدروژن
ارسال شده: پنجشنبه ۱۴۰۲/۱/۱۷ - ۱۴:۰۳
توسط decoder
MRT نوشته شده: ↑سهشنبه ۱۴۰۲/۱/۱۵ - ۲۱:۴۴
انرژی جنبشی آنها به صورت امواج الکترومغناطیس تابش می کند
همانطور كه میدانیم میانگین سرعت حركت ملكولهای گاز نیتروژن در دمای اتاق و فشار یك اتمسفر 5.5 متر بر ثانیه است كه مسلما با كاهش دما ، این سرعت كاهش پیدا می كند ولی تصادم ملكولهای گاز با یكدیگر اجتناب ناپذیر است و این تصادمها ایجاد حرارت هر چند كم ولی امواج الكترومغناطیس تولید و منتشر می كند كه میتواند نامزد مناسبی برای منشاء امواج پس زمینه كیهانی نیز باشد . چرا كه توده های گاز هیدروژن و هلیم در كیهان به طور گسترده ای پراكنده شده است.

Q مقدار انرژی لازم جهت افزایش یك درجه كلوین جهت یك كیلوگرم گاز هیدروژن را نشان می دهد .
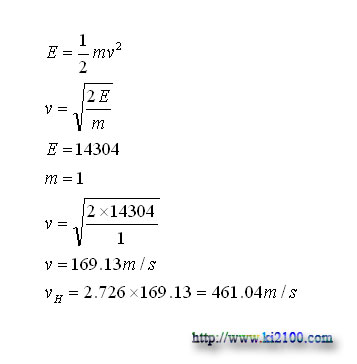
VH سرعت حركت محاسبه شده برای اتمهای هیدروژن جهت تامین این مقدار انرژی لازم است ( تبدیل انرژی جنبشی به حرارتی به علت برخورد و تصادم ) كه با در نظر گرفتن فشار پایین در فضا و شرایط محیطی منجمله فعالیت شدید ستارگان ، چرخش و حركت اجرام در فضا ، میادین الكترومغناطیسی و ... بسیار محتمل و ممكن به نظر میرسد. اینك اگر تصادم شاخ به شاخ دو اتم هیدروژن را در نظر بگیریم سرعت به 326 متر بر ثانیه كاهش پیدا می كند و اگر تصادم دو ملكول هیدروژن را در نظر بگیریم سرعت به 230.53 متر بر ثانیه كاهش پیدا خواهد کرد.
طبق چیزی که گفتین فرض کنین این انرژی دریافتی صرف انتقال الکترون به لایه های بالاتر بشه. این الکترون تا چه مدت توی اون لایه و به حالت بر انگیخته باقی میمونه؟ نیم عمر این انتقال چقدره؟ اگر دما رو کاهش بدیم نیم عمر افزایش پیدا میکنه؟؟
Re: برخورد دو اتم هیدروژن
ارسال شده: پنجشنبه ۱۴۰۲/۱/۱۷ - ۱۴:۱۹
توسط MRT
تا زمانی که انرژی جذب لایه پایین تر نشود. یعنی اگر توسط آن لایه انرژی کوانتومی جذب نشود الکترون با پس دادن انرژی به لایه قبلی خود بر می گردد. این دو مقاله را بخوانید
اصل تبادل انرژي كوانتومي توسط لايهها و زير لايهها در اتمها
https://ki2100.com/physics/quantum.htm
فوتون ذره اي يا رشته اي ، فوتون يك ثانيه اي يا چند ثانيه اي ، كوانتيده شدن انرژي در همبافته فضا - زمان
https://ki2100.com/physics/Photon_P_t.htm
ولی این بحثی که ما راه انداختیم کلاسیک است. در فیزیک کوانتوم خود الکترون یک نوع جرم تابشی و همانند موج در پیرامون هسته حل می شود. و بحث کلی تداخل دو موج الکترون و موج فوتون است. این بحث قبلی مربوط به نظریه بور است که بعدها نظریه شرودینگر جایش را گرفت.
انرژی جنبشی الکترون در تراز ضربدر عدد کوانتومی n

انرژی فوتون