ویژگیهای اصلی انبساط حرارتی چیست؟ اول ، انبساط حرارتی به وضوح با تغییر دما مرتبط است. هرچه تغییر دما بیشتر باشد ، نوار دو فلزی بیشتر خم می شود. دوم ، بستگی به مواد دارد. به عنوان مثال ، در دماسنج ، انبساط الکل بسیار بیشتر از انبساط شیشه حاوی آن است.
علت اصلی انبساط حرارتی چیست؟ همانطور که در نظریه سینتیک توضیح داده شده است: توضیح اتمی و مولکولی فشار و دما ، افزایش دما به معنی افزایش انرژی جنبشی تک اتم ها است. در یک جامد ، برخلاف گاز ، اتم ها یا مولکول ها به هم نزدیک هستند ، اما انرژی جنبشی آنها (به شکل ارتعاشات کوچک و سریع) اتم ها یا مولکول های مجاور را از یکدیگر جدا می کند. این هل دادن همسایه به همسایه به طور متوسط فاصله کمی بیشتر بین همسایه ها ایجاد می کند و اندازه بزرگتری برای کل بدن ایجاد می کند. برای اکثر مواد تحت شرایط عادی ، جهت مطلوبی وجود ندارد و افزایش دما باعث افزایش اندازه جامد در هر بعد به میزان معینی می شود.
انبساط حرارتی چیست؟انبساط حرارتی ناشی از ماهیت نامتقارن بودن منحنی انرژی بالقوه برای اتم ها در یک جامد است. اگر نوسان سازها واقعاً هارمونیک بودند ، فارغ از دامنه ارتعاش تغییر نمی کرد.
من نمی فهمم که اگر نوسانات هارمونیک باشند ، ممکن است افزایش دما بر حجم یک ماده جامد تأثیر نگذارد؟اگر پتانسیل بین اتمی یک سهمی کامل باشد ، این درست است که هیچ انبساط حرارتی وجود نخواهد داشت. چرا؟ خوب ، با ارتعاش بیشتر و بیشتر اتمها ، موقعیت متوسط اتم تغییر نمی کند. مطمئناً بیشتر تکان می خورد ، اما به همان اندازه در یک طرف تکان می خورد. تغییر در موقعیت متوسط اتمی صفر خواهد بود. در مقابل ، اگر پتانسیل کج باشد (همانطور که برای یک پتانسیل بین اتمی است) ، زمان متوسط موقعیت اتمی با افزایش دامنه ارتعاش تغییر می کند. به طور متوسط ، با افزایش دما (معمولاً) به فاصله بین اتمی بیشتری حرکت می کند.
البته ، این فرایند نه در تمام دماها خطی است و نه لزوماً یکنواخت است ، همانطور که توسط بسیاری از مواد واقعی نشان داده شده است.اینها انرژی بالقوه در برابر نمودارهای جداسازی اتمی هستند.
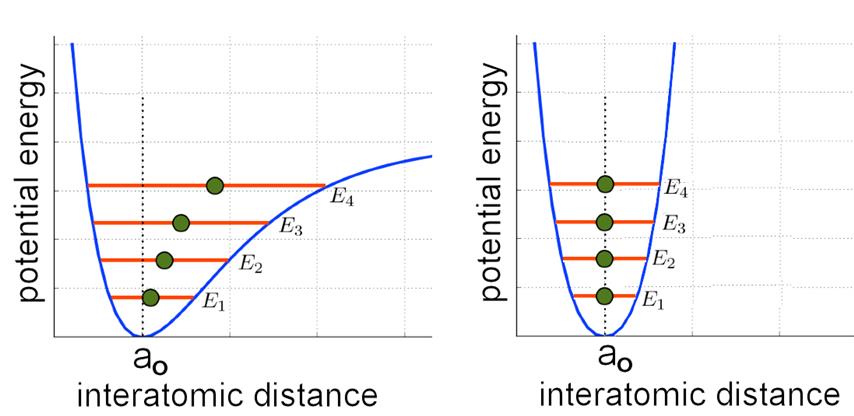
وقتی اتم ارتعاشی نباشد ، فاصله تعادل بین اتمها $a_{\rm o}$ است.
با افزایش دما انرژی جنبشی ، $E_!, E_2, E_3, E_4, E_5$اتم ها افزایش می یابد و دامنه ارتعاش آنها افزایش می یابد.
برای یک پتانسیل متقارن ، مانند سمت راست ، میانگین جداسازی اتمها ، که توسط لکه های سبز نشان داده شده است ، در ao یکسان می ماند و مواد منبسط نمی شوند.با این حال ، برای یک نمودار بالقوه نامتقارن ، همانطور که در سمت چپ نشان داده شده است ، میانگین جداسازی اتم ها افزایش می یابد و به تدریج بزرگتر از $a_{\rm o}$ می شود و مواد گسترش می یابد.
چرا یک ماده با انجماد منبسط می شود؟ چه شرایطی این امر را ضروری می کند؟دلیل این امر ، به بیان ساده ، ساختار شبکه ای است که مولکول ها هنگام انجماد تشکیل می دهند. برای موادی که با انجماد این انبساط را نشان می دهند ، ساختار شبکه بیشتر از زمانی که مایع است ، فضای بیشتری را اشغال می کند. به عنوان مثال ، آب (به دلیل شکل گیری/زاویه پیوندهای هیدروژنی با اتم اکسیژن) هنگام یخ زدگی دارای ساختار شبکه ای شش ضلعی است که فضای بسیار بیشتری را نسبت به حالت رومینگ مولکول آب مایع اش اشغال می کند.
آیا دما بر ظرفیت گرمایی تأثیر می گذارد؟ظرفیت گرمایی شیب نمودار انرژی داخلی U با درجه حرارت T. انرژی داخلی انرژی است که در اثر چرخش و انرژی ارتعاشی یک مولکول دارای آن است و با افزایش دما سطوح انرژی چرخشی و ارتعاشی بیشتر تحریک می شود و بنابراین داخلی انرژی افزایش می یابد
در ابتدا انرژی داخلی کوچک است و با افزودن انرژی به آرامی تغییر می کند ، عمدتا به این دلیل که انرژی کافی برای تحریک بسیاری از چرخش ها یا ارتعاشات وجود ندارد. بنابراین شیب U در مقابل T کوچک است و ظرفیت گرمایی نیز کوچک است. سپس با افزایش دما بیشتر سطوح انرژی برانگیخته می شود و انرژی داخلی به سرعت افزایش می یابد و همچنین شیب U در مقابل T افزایش می یابد و بنابراین ظرفیت گرمایی افزایش می یابد.
در دماهای بسیار بالا ، بسیاری از سطوح انرژی پر شده و بنابراین میزان افزایش با افزایش دما ثابت می شود و بنابراین ظرفیت گرمایی ثابت می شود ، یعنی به حداکثر مقدار می رسد. این نمودار تغییر ظرفیت حرارتی با انرژی را فقط برای سطوح ارتعاشی نشان می دهد ، اما هنگامی که انرژی چرخشی و انتقالی به آن اضافه می شود ، شکل کلی یکسانی دارد.
انرژی داخلی در برابر دما
ظرفیت حرارتی ارتعاشی در مقابل دما
منطقه دمای پایین ظرفیت گرما در مقابل دما. نمودار دست انداز به دلیل مقادیر گسسته سطوح انرژی ارتعاشی است.I hope I help you understand the question. Roham Hesami






