الکترولیز آب تحت فشار
الکترولیز آب تحت فشار
سلام . فرض کنیم با کمپرسور یه مخزنی با تحمل فشار بالا رو با هوای فشرده پر میکنیم . هرچی مخزن فشارش بیشتر میشه برای ادامه فشرده سازی کمپرسور نیاز به موتور قویتر و مصرف انرژی بیشتری دارد.
حالا فرض کنیم مخزن با اکسیژن و هیدروژنی که از الکترولیز اب بدست میاد در حال پر شدن هست و فشارش افزایش پیدا میکنه ولی ظاهرا انرژی که دستگاه الکترولیز مصرف میکند همچنان تابعی از زمان هست و ربطی به فشار ندارد (از تاثیر میزان حلالیت این دو گاز در اب بر اثر فشار و تاثیرش بر الکترولیز صرف نظر میکنیم)
یعنی ما با یه مقدار کمتر انرژی تونستیم فشار بسیار بالایی ایجاد کنیم
سوال : به نظر شما مخلوط اکسیژن و هیدروژن تحت فشار بالا امکان خودسوزی بدون جرقه را دارد یا میشه این فشرده سازی رو تا حدی که مخزن تحمل کنه بالا برد. ایا میشه از این مورد استفاده ای کرد
حالا فرض کنیم مخزن با اکسیژن و هیدروژنی که از الکترولیز اب بدست میاد در حال پر شدن هست و فشارش افزایش پیدا میکنه ولی ظاهرا انرژی که دستگاه الکترولیز مصرف میکند همچنان تابعی از زمان هست و ربطی به فشار ندارد (از تاثیر میزان حلالیت این دو گاز در اب بر اثر فشار و تاثیرش بر الکترولیز صرف نظر میکنیم)
یعنی ما با یه مقدار کمتر انرژی تونستیم فشار بسیار بالایی ایجاد کنیم
سوال : به نظر شما مخلوط اکسیژن و هیدروژن تحت فشار بالا امکان خودسوزی بدون جرقه را دارد یا میشه این فشرده سازی رو تا حدی که مخزن تحمل کنه بالا برد. ایا میشه از این مورد استفاده ای کرد
- rohamavation
نام: roham hesami radرهام حسامی راد
محل اقامت: 100 مایلی شمال لندن جاده آیلستون، لستر، لسترشر. LE2
عضویت : سهشنبه ۱۳۹۹/۸/۲۰ - ۰۸:۳۴
پست: 3286-
سپاس: 5494
- جنسیت:
تماس:
Re: الکترولیز آب تحت فشار
در سرعت فشار بر مولکول آب میزان انرژی مورد نیاز را تعیین می کند. بنابراین افزایش فشار به معنای نیاز به انرژی بیشتر خواهد بود.
یک محیط با فشار بالا مایعات را نسبت به گازها ترجیح می دهد ، تا آنجا که مایعات از چگالی بیشتری برخوردار هستند. بنابراین هرچه فشار بیشتر باشد ، برای ایجاد واکنش H2O -> H2 + O2 باید ولتاژ بیشتری اعمال کنید.
اما ، با ولتاژ کافی بالا ، همیشه باید امکان پذیر باشد. اگر ولتاژ را به اندازه کافی بالا برسانید ، در نهایت هر واکنش الکترولیتی رخ خواهد داد. اگر واکنش های رقیب ترجیح داده شوند ، الکترولیز فقط (در عمل) غیرممکن می شود (در هر ولتاژ) من مطمئن نیستم که واکنش های رقیب برای الکترولیز کردن آب خالص در یک محیط با فشار بالا چه خواهد بود. به عنوان مثال ، احتمالاً H2O -> H2 + O3 (گاز ازن) نسبت به H2O -> H2 + O2 با فشار کافی بالا ترجیح داده می شود.
در اینجا کمی بودن غیرممکن است ، زیرا مکانیزم کاتالیزور و واکنش نیز تفاوت زیادی ایجاد می کند تا یک واکنش را نسبت به واکنش دیگر ترجیح دهد. فقط محاسبه انرژی های آزاد کافی نیست.
برای هر گاز حداکثر ضریب تراکم (Q) وجود دارد. و از آنجا که دو محصول هیدروژن و اکسیژن داریم ، کمترین مقدار (Q) را برای اکسیژن داریم ، بنابراین در صورت الکترولیز آب تحت فشار زیاد ، انتظار می رود با رسیدن فشار داخل (Q) واکنش شما متوقف شود. اکنون (Q) را پیدا کنید. چگونه این کار را انجام می دهیم؟ البته هیدروژن و اکسیژن شما برگشت پذیر بوده در اب حل میشود .
یک محیط با فشار بالا مایعات را نسبت به گازها ترجیح می دهد ، تا آنجا که مایعات از چگالی بیشتری برخوردار هستند. بنابراین هرچه فشار بیشتر باشد ، برای ایجاد واکنش H2O -> H2 + O2 باید ولتاژ بیشتری اعمال کنید.
اما ، با ولتاژ کافی بالا ، همیشه باید امکان پذیر باشد. اگر ولتاژ را به اندازه کافی بالا برسانید ، در نهایت هر واکنش الکترولیتی رخ خواهد داد. اگر واکنش های رقیب ترجیح داده شوند ، الکترولیز فقط (در عمل) غیرممکن می شود (در هر ولتاژ) من مطمئن نیستم که واکنش های رقیب برای الکترولیز کردن آب خالص در یک محیط با فشار بالا چه خواهد بود. به عنوان مثال ، احتمالاً H2O -> H2 + O3 (گاز ازن) نسبت به H2O -> H2 + O2 با فشار کافی بالا ترجیح داده می شود.
در اینجا کمی بودن غیرممکن است ، زیرا مکانیزم کاتالیزور و واکنش نیز تفاوت زیادی ایجاد می کند تا یک واکنش را نسبت به واکنش دیگر ترجیح دهد. فقط محاسبه انرژی های آزاد کافی نیست.
برای هر گاز حداکثر ضریب تراکم (Q) وجود دارد. و از آنجا که دو محصول هیدروژن و اکسیژن داریم ، کمترین مقدار (Q) را برای اکسیژن داریم ، بنابراین در صورت الکترولیز آب تحت فشار زیاد ، انتظار می رود با رسیدن فشار داخل (Q) واکنش شما متوقف شود. اکنون (Q) را پیدا کنید. چگونه این کار را انجام می دهیم؟ البته هیدروژن و اکسیژن شما برگشت پذیر بوده در اب حل میشود .

-
sohrab 4242
نام: سهراب نعمتی
عضویت : سهشنبه ۱۴۰۱/۹/۸ - ۲۱:۴۷
پست: 11-
- جنسیت:
Re: الکترولیز آب تحت فشار
سلام فشار آب در اعماق ده کیلومتری زیر آب تقریبا ده تن بر متر مربع است برای الکترولیز آب تحت چنین فشاری چه توان الکتریکی لازم است چقدر اختلاف با الکترولیز در سطح آب دارد ممنون
- rohamavation
نام: roham hesami radرهام حسامی راد
محل اقامت: 100 مایلی شمال لندن جاده آیلستون، لستر، لسترشر. LE2
عضویت : سهشنبه ۱۳۹۹/۸/۲۰ - ۰۸:۳۴
پست: 3286-
سپاس: 5494
- جنسیت:
تماس:
Re: الکترولیز آب تحت فشار
با افزایش فشار، راندمان الکترولیز به طور کلی کاهش پیدا میکنه. اما در فشار پایین (از 1 اتمسفر به 5 اتمسفر) و چگالی جریان بالا افزایش می یابه . نتایج نشان می دهد که ولتاژ سلول به زیر 8 اتمسفر افزایش می یابد و سپس با فشار کاری کاهش می یابد. علاوه بر این، اثرات شرایط مرزی عایق حرارتی، پیکربندی جریان گاز و میزان استفاده از گاز تحت فشارهای عملیاتی مختلف نیز مورد بحث قرار میگیرد. مشخص شده است که واکنش اصلاح داخلی مستقیم معکوس تحت فشار عملیاتی بالاتر از 3 اتمسفر فعال می شود. علاوه بر این، در مقایسه با آرایش همجریان، آرایش جریان مخالف برای بهبود عملکرد سلول در چگالی جریان بالا مفیدتر است.در حالت شدید که فشار اتمسفر به صفر کاهش می یابد (خلاء)، تمام آب می جوشد و الکترولیز متوقف می شود.
برای حالت شدید دیگر، جایی که فشار اتمسفر به بالای 1 گیگا پاسکال افزایش مییابد، آب به یخ تبدیل میشود و الکترولیز متوقف میشود.فشار اتمسفر حتی در فشارهای معتدل تر از موارد شدیدی تأثیراتی بر کارایی خواهد داشت.
اولی یک اثر ترمودینامیکی است - جو حاوی اکسیژن است که محصول الکترولیز آب است. با افزایش فشار اتمسفر، مقدار اکسیژن حل شده در الکترولیت را نیز افزایش می دهید و این باعث می شود که تولید اکسیژن کمی کمتر شود (ولتاژ بالاتری لازم است). ولتاژ مورد نیاز برای هدایت واکنش تولید اکسیژن (مانند تمام نیمه واکنشهای الکتروشیمیایی) به غلظت محصول و واکنشدهنده مربوط میشود (نگاه کنید به: برای واکنش $2 H2O → O2 + 4 H+ + 4 e–$
$E = E0 - (R*T*ln([H2O]2*[O2]–1*[H+]–4))/F$
که در آن R ثابت گاز جهانی، T دمای مطلق، F عدد فارادی است، و [چیزی] نشان دهنده غلظت چیزی است.
اثر دوم بیشتر جنبه مهندسی دارد - هر چه فشار بیشتر باشد، حجم حباب های تولید شده کمتر می شود (نسبت معکوس). این بدان معناست که برای سرعت معینی از تولید هیدروژن و اکسیژن، کمتر از هر الکترود توسط حبابها (که عایقهای مؤثر هستند و واکنش را مسدود میکنند) پوشیده میشود. یا، در فشارهای بالاتر، می توانید محصول بیشتری را در واحد سطح نسبت به سطح پایین تشکیل دهید.
تغییر کلی در راندمان، با توجه به این اثرات رقابتی، تعیین کمیت آن دشوار خواهد بود، زیرا تابعی از دما، فشار، pH، سطح الکترود، ولتاژ اعمال شده، هدایت محلول و احتمالاً چند پارامتر دیگر است که نمیتوانم انجام دهم. در لحظه فکر کن
در فشارهای معقول، هر دو اثر حداقل هستند. اگر می خواهید راندمان الکترولیز خود را به میزان قابل توجهی افزایش دهید، ساده ترین متغیرهایی که می توانید با آنها بازی کنید ترکیب الکترولیت، مواد الکترود و هندسه سلول است.
وارد شده استیک نقطه نگرانی تولید هیدروژن تحت فشار زیاد.
تحت فشار فزاینده، هم هیدروژن و هم اکسیژن به طور فزاینده ای در آب پخش می شوند، سپس به ستون های مقابل، و از مخلوط شدن با گازهای ستون دیگر جلوگیری می کنند. این باعث میشود که حفظ خلوص ستونهای گاز مربوطه سختتر شود و مهمتر از آن، ایمن باشد.
کسی نمیخواهد بمبی بالقوه با مقادیر انفجاری هیدروژن در کلمب اکسیژن، و یا مقادیر انفجاری اکسیژن در کلمب هیدروژنی، تحت فشارهای معمولی، چه رسد به فشارهای زیاد، بسازد.
در واقع، حتی در فشارهای پایین، با توجه به زمان کافی، انتشار باعث اختلاط گازها می شود. خلوص نسبی هم به میزان تولید و هم به سرعت انتشار مربوط می شود.بالاترین فشار آبی که می توان در آن الکترولیز انجام داد چیست؟
بالاترین فشار آبی که در آن الکترولیز می توان برای استخراج هیدروژن و اکسیژن انجام داد چیست؟ آیا ثابت دی الکتریک آب که با افزایش فشار کاهش می یابد در این امر تأثیری دارد؟یک محیط پرفشار تمایل دارد مایعات را بر گازها ترجیح دهد، تا جایی که مایعات چگالی بالاتری دارند. بنابراین هر چه فشار بیشتر باشد، ولتاژ بیشتری باید اعمال کنید تا واکنش H2O --> H2+O2 رخ دهد.
اما، با ولتاژ به اندازه کافی بالا، همیشه باید امکان پذیر باشد. اگر ولتاژ را به اندازه کافی بالا ببرید، در نهایت هر واکنش الکترولیتی رخ خواهد داد. الکترولیز فقط در صورتی غیرممکن می شود (در عمل) (در هر ولتاژی غیرممکن است)، اگر واکنش های رقیب مورد علاقه باشد. من مطمئن نیستم که واکنش های رقابتی برای الکترولیز آب خالص در یک محیط پرفشار چه خواهد بود. به عنوان مثال، احتمالاً H2O --> H2 + O3 (گاز ازن) در فشار کافی بالا بر H2O --> H2 + O2 ترجیح داده می شود.
در اینجا غیرممکن است که کمی باشد، زیرا مکانیسم کاتالیزور و واکنش نیز تفاوت بزرگی برای برتری یک واکنش بر واکنش دیگر ایجاد می کند. فقط محاسبه انرژی های آزاد کافی نیست.
برای هر گاز حداکثر ضریب تراکم پذیری (Q) وجود دارد. و از آنجایی که ما دو محصول هیدروژن و اکسیژن داریم، کمترین (Q) را که برای اکسیژن است پیش میرویم، بنابراین در صورت الکترولیز آب تحت فشار بالا، انتظار دارید واکنش شما با رسیدن فشار داخل (Q) متوقف شود. اکنون برای پیدا کردن (Q). چگونه این کار را انجام دهیم؟ برای یک گاز باید ببینید چگالی آن زمانی که مایع است چقدر است (به عنوان مثال لیتر در کیلوگرم) سپس پنجمین آن باید حداکثر چگالی باشد که می توانید با هر فشاری به دست آورید زیرا پس از آن فشار باعث ایجاد اتم ها می شود. تاثیر فشار بر الکترولیز آب آب دریا با افزایش عمق چیست؟ فرض کنید من در حال حاضر روی یک ربات زیر آب کار می کنم و امیدوار هستم که از حباب های گاز تولید شده توسط الکترولیز آب برای کنترل شناوری استفاده کنم. عمق عملیاتی بین 200 تا 1000 متر است.هر چه فشار بیشتر باشد کار را بسیار دشوارتر می کند. ولی...
برای الکترولیز آب به الکترودهایی با پتانسیل زیاد، ترجیحاً بزرگ با فاصله الکترودهای کوچک بین آنها نیاز دارید. شما می خواهید آب شفاف و صاف شده و بدون برق گرفتگی ماهی ها، تمام زیردریایی را به دلیل اتصال کوتاه تصادفی بسوزانید.
و برای کنترل شناوری به گاز زیادی نیاز خواهید داشت، به خصوص در اعماق 200-1000 متر، بنابراین به برق زیادی نیاز دارید:
طبق قانون فارادی
$m=(Q/F)(M/z)$
که در آن $F = 96485\ \mathrm{C/mol}$ می توانید مانند 4.5 لیتر گاز هیدروژن (1 اتمسفر، 25 درجه سانتی گراد) با جریان 10 آمپر در 1 ساعت بسازید! این معادل 0.04 لیتر در 1000 متر (100 اتمسفر) گاز بالقوه انفجار است.
آیا حجم آب درگیر بر سرعت الکترولیز تأثیر می گذارد؟من در حال کار بر روی طراحی یک الکترولیز PEM خانگی هستم و هدف من این است که آن را تا حد امکان فشرده کنم تا امکان حمل و نقل آسان را فراهم کنم. سوال من، همانطور که به آن مربوط می شود، این است که آیا - با همان جریان اعمال شده - حجم آب داخل الکترولیز بر سرعت تجزیه به H2 و O2 تأثیر می گذارد؟عوامل زیادی وجود دارد که بر نرخ تأثیر می گذارد، به عنوان مثال. مساحت، فاصله و نوع الکترودها، الکترولیت، چگالی جریان و جریان، و غیره. اما، اگر تنها عامل تغییر حجم بود (یعنی الکترودها کاملاً غوطه ور هستند و همیشه در بالای محلول روی یک شناور هستند، نه در پایین محلول که فشار وجود دارد. ممکن است تغییر کند)، حجم در ابتدا تأثیری نخواهد داشت.
با این حال، همانطور که واکنش ادامه می یابد و غلظت الکترولیت شروع به تغییر می کند، به دلیل از دست دادن آب و احتمالاً به دلیل انحلال الکترودها، غلظت با حجم زیاد الکترولیت کندتر تغییر می کند. بنابراین، ممکن است یک تفاوت مرتبه دوم با ادامه الکترولیز وجود داشته باشد.
آیا تغییر غلظت الکترولیت در الکترولیز آب بر سرعت تولید گاز هیدروژن در کاتد تأثیر می گذارد؟با کاهش غلظت الکترولیت، یا ولتاژ مورد نیاز در جریان ثابت افزایش می یابد، یا جریان عبوری در ولتاژ ثابت کاهش می یابد.
هر دو به این دلیل اتفاق میافتند که در غلظتهای پایینتر، گرادیان پتانسیل بالاتری در الکترولیت برای حفظ جریان یکسان مورد نیاز است، زیرا تعداد یونهای کوچکتر نیاز به حرکت سریعتر یونها برای همان جریان دارد.
این گرادیان پتانسیل و افت پتانسیل ناشی از آن در برابر ولتاژ خارجی عمل می کند. پتانسیل های الکترود اجباری را به پتانسیل تعادل آنها نزدیک می کند. سپس واکنشهای الکترود خالص کندتر میشوند.
چگونه آنها الکترولیز را در گرانش صفر انجام می دهند؟اساساً، من تصور می کنم که انجام الکترولیز در گرانش صفر دشوار است، زیرا شما اساساً تمام کنترل خود را در مورد جایی که گاز خروجی می رود از دست می دهید. چگونه این را حل می کنند؟من حدس میزنم پاسخ کلی برای هر سیستم جداسازی جرمی این باشد که شما آن را بچرخانید، اما جداسازی جرم واقعاً برای الکترولیز مؤثر نیست، زیرا این جداسازی بیشتر بین آند و کاتد نیاز دارد که منجر به تلفات اهمی پروتونیک، یعنی افزایش مقاومت داخلی میشود. بنابراین جداسازی بهینه گونه ها نه با جرم آنها، بلکه با اندازه و بار آنها، معمولاً از طریق یک غشای تبادل پروتون (PEM) انجام می شود.
الکترولیز PEM امکان قرار دادن الکترود محکمتر را برای کاهش تلفات اهمی فراهم میکند، جریان بالاتری را امکانپذیر میکند و در برابر فشارهای نسبتاً بالا متحمل است. آب اگر از انتهای آند تغذیه شود و با جریان از کاتد به سمت آند، آب به هیدروژن و اکسیژن جدا می شود، هیدروژن با بار مثبت از طریق PEM به سمت کاتد با بار منفی جذب می شود و اکسیژن با بار منفی از کاتد به سمت آند دفع می شود. آند با بار مثبت:
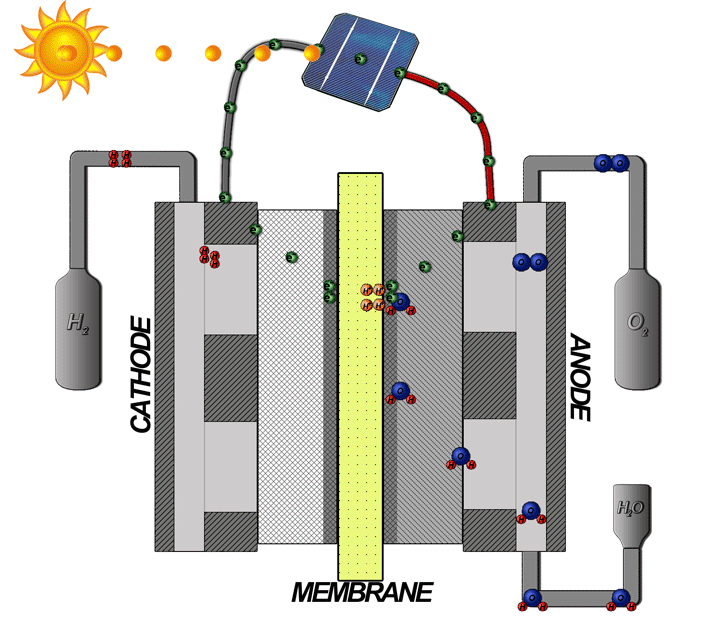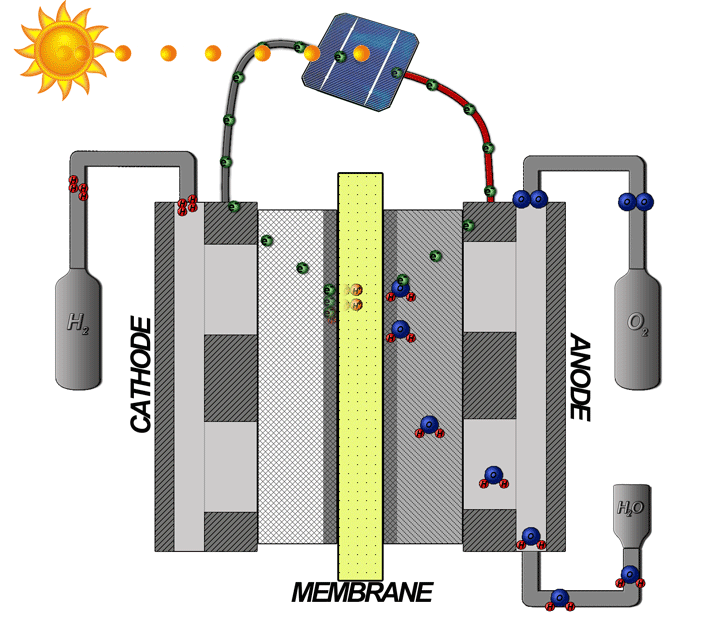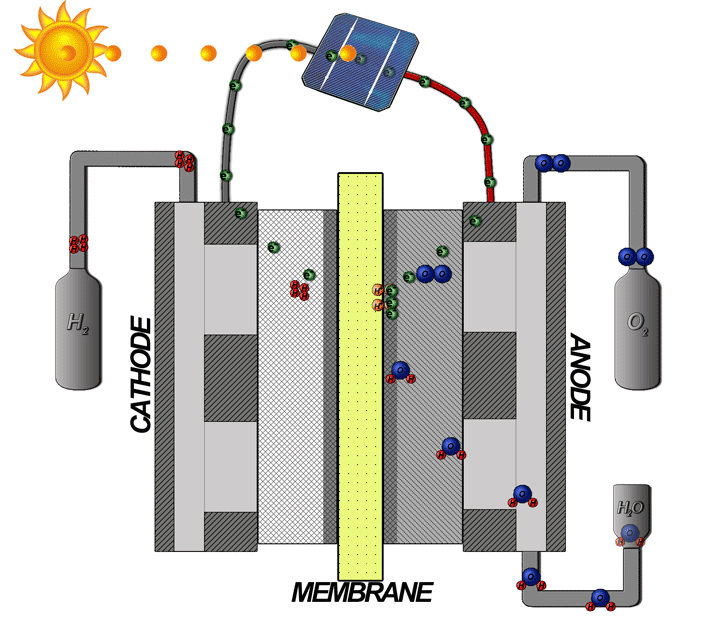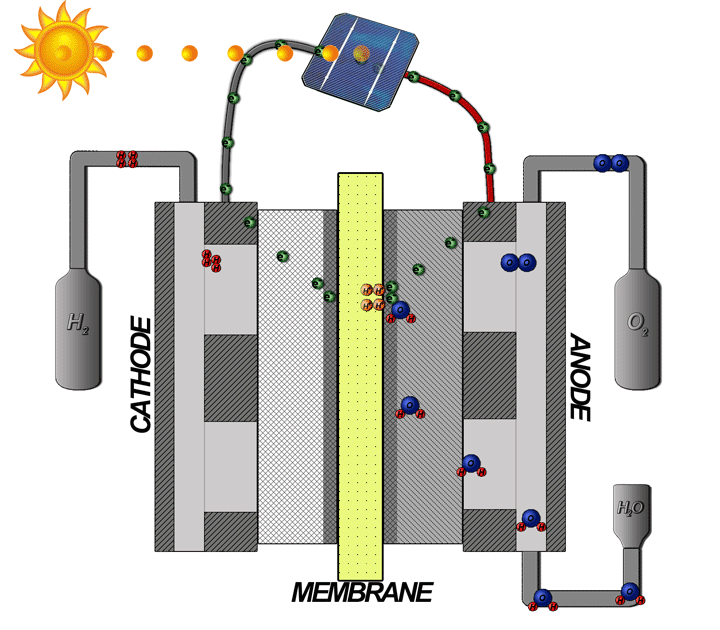
الکترولیز PEM منبع اصلی اکسیژن در ایستگاه فضایی بینالمللی است و از شمعهای پرکلرات به عنوان پشتیبان (برای مواقع اضطراری یا زمانی که دستگاه الکترولیز کار نمیکند) استفاده میکند.
ژنراتور بر اساس یک اصل ساده کار می کند - الکترولیز، تفکیک اکسیژن و هیدروژن از آب از طریق استفاده از برق. چه چیزی ژنراتور را ایمن می کند؟ این دستگاه از یک غشای تبادل پروتون (PEM) برای جداسازی هیدروژن و اکسیژن تولید شده استفاده می کند.
در الکترولایزر PEM، آب در الکترود اکسیژن یا آند سلولی اکسید میشود تا گاز اکسیژن تولید کند و یونهای هیدروژن (پروتون) و الکترونها آزاد شود. یون های هیدروژن از آند سلول به کاتد سلول یا الکترود هیدروژن تحت تأثیر میدان الکتریکی اعمال شده در سراسر سلول مهاجرت می کنند، در حالی که الکترون ها توسط یک منبع برق dc منتقل می شوند. پروتون ها و الکترون ها در کاتد سلول دوباره ترکیب می شوند و هیدروژن تولید می کنند. آب مایع نیز در کاتد به دلیل فرآیندی به نام درگ الکترواسموتیک آزاد می شود. اکسیژن و هیدروژن در یک نسبت استوکیومتری - دو واحد حجمی هیدروژن برای هر یک از اکسیژن - با نرخی متناسب با جریان سلول اعمال شده تولید می شوند.
تولید هیدروژن تحت فشار در زیر آب و سپس استفاده از آن برای انجام کار
همانطور که حدس زدید، این کار نمی کند زیرا الکترولیز آب در فشار بالا دشوارتر است. طبق معادله نرنست، تغییر انرژی آزاد گیبس (و در نتیجه ولتاژ مورد نیاز) برای یک واکنش الکتروشیمیایی به غلظت واکنش دهنده ها و محصولات بستگی دارد. غلظت گاز با فشار جزئی آن اندازه گیری می شود. در این حالت، واکنش در عمق بیشتر نامطلوب تر می شود، زیرا غلظت آب به سختی تغییر می کند در حالی که فشار گازهای محصول (هیدروژن و اکسیژن) افزایش می یابد
برای حالت شدید دیگر، جایی که فشار اتمسفر به بالای 1 گیگا پاسکال افزایش مییابد، آب به یخ تبدیل میشود و الکترولیز متوقف میشود.فشار اتمسفر حتی در فشارهای معتدل تر از موارد شدیدی تأثیراتی بر کارایی خواهد داشت.
اولی یک اثر ترمودینامیکی است - جو حاوی اکسیژن است که محصول الکترولیز آب است. با افزایش فشار اتمسفر، مقدار اکسیژن حل شده در الکترولیت را نیز افزایش می دهید و این باعث می شود که تولید اکسیژن کمی کمتر شود (ولتاژ بالاتری لازم است). ولتاژ مورد نیاز برای هدایت واکنش تولید اکسیژن (مانند تمام نیمه واکنشهای الکتروشیمیایی) به غلظت محصول و واکنشدهنده مربوط میشود (نگاه کنید به: برای واکنش $2 H2O → O2 + 4 H+ + 4 e–$
$E = E0 - (R*T*ln([H2O]2*[O2]–1*[H+]–4))/F$
که در آن R ثابت گاز جهانی، T دمای مطلق، F عدد فارادی است، و [چیزی] نشان دهنده غلظت چیزی است.
اثر دوم بیشتر جنبه مهندسی دارد - هر چه فشار بیشتر باشد، حجم حباب های تولید شده کمتر می شود (نسبت معکوس). این بدان معناست که برای سرعت معینی از تولید هیدروژن و اکسیژن، کمتر از هر الکترود توسط حبابها (که عایقهای مؤثر هستند و واکنش را مسدود میکنند) پوشیده میشود. یا، در فشارهای بالاتر، می توانید محصول بیشتری را در واحد سطح نسبت به سطح پایین تشکیل دهید.
تغییر کلی در راندمان، با توجه به این اثرات رقابتی، تعیین کمیت آن دشوار خواهد بود، زیرا تابعی از دما، فشار، pH، سطح الکترود، ولتاژ اعمال شده، هدایت محلول و احتمالاً چند پارامتر دیگر است که نمیتوانم انجام دهم. در لحظه فکر کن
در فشارهای معقول، هر دو اثر حداقل هستند. اگر می خواهید راندمان الکترولیز خود را به میزان قابل توجهی افزایش دهید، ساده ترین متغیرهایی که می توانید با آنها بازی کنید ترکیب الکترولیت، مواد الکترود و هندسه سلول است.
وارد شده استیک نقطه نگرانی تولید هیدروژن تحت فشار زیاد.
تحت فشار فزاینده، هم هیدروژن و هم اکسیژن به طور فزاینده ای در آب پخش می شوند، سپس به ستون های مقابل، و از مخلوط شدن با گازهای ستون دیگر جلوگیری می کنند. این باعث میشود که حفظ خلوص ستونهای گاز مربوطه سختتر شود و مهمتر از آن، ایمن باشد.
کسی نمیخواهد بمبی بالقوه با مقادیر انفجاری هیدروژن در کلمب اکسیژن، و یا مقادیر انفجاری اکسیژن در کلمب هیدروژنی، تحت فشارهای معمولی، چه رسد به فشارهای زیاد، بسازد.
در واقع، حتی در فشارهای پایین، با توجه به زمان کافی، انتشار باعث اختلاط گازها می شود. خلوص نسبی هم به میزان تولید و هم به سرعت انتشار مربوط می شود.بالاترین فشار آبی که می توان در آن الکترولیز انجام داد چیست؟
بالاترین فشار آبی که در آن الکترولیز می توان برای استخراج هیدروژن و اکسیژن انجام داد چیست؟ آیا ثابت دی الکتریک آب که با افزایش فشار کاهش می یابد در این امر تأثیری دارد؟یک محیط پرفشار تمایل دارد مایعات را بر گازها ترجیح دهد، تا جایی که مایعات چگالی بالاتری دارند. بنابراین هر چه فشار بیشتر باشد، ولتاژ بیشتری باید اعمال کنید تا واکنش H2O --> H2+O2 رخ دهد.
اما، با ولتاژ به اندازه کافی بالا، همیشه باید امکان پذیر باشد. اگر ولتاژ را به اندازه کافی بالا ببرید، در نهایت هر واکنش الکترولیتی رخ خواهد داد. الکترولیز فقط در صورتی غیرممکن می شود (در عمل) (در هر ولتاژی غیرممکن است)، اگر واکنش های رقیب مورد علاقه باشد. من مطمئن نیستم که واکنش های رقابتی برای الکترولیز آب خالص در یک محیط پرفشار چه خواهد بود. به عنوان مثال، احتمالاً H2O --> H2 + O3 (گاز ازن) در فشار کافی بالا بر H2O --> H2 + O2 ترجیح داده می شود.
در اینجا غیرممکن است که کمی باشد، زیرا مکانیسم کاتالیزور و واکنش نیز تفاوت بزرگی برای برتری یک واکنش بر واکنش دیگر ایجاد می کند. فقط محاسبه انرژی های آزاد کافی نیست.
برای هر گاز حداکثر ضریب تراکم پذیری (Q) وجود دارد. و از آنجایی که ما دو محصول هیدروژن و اکسیژن داریم، کمترین (Q) را که برای اکسیژن است پیش میرویم، بنابراین در صورت الکترولیز آب تحت فشار بالا، انتظار دارید واکنش شما با رسیدن فشار داخل (Q) متوقف شود. اکنون برای پیدا کردن (Q). چگونه این کار را انجام دهیم؟ برای یک گاز باید ببینید چگالی آن زمانی که مایع است چقدر است (به عنوان مثال لیتر در کیلوگرم) سپس پنجمین آن باید حداکثر چگالی باشد که می توانید با هر فشاری به دست آورید زیرا پس از آن فشار باعث ایجاد اتم ها می شود. تاثیر فشار بر الکترولیز آب آب دریا با افزایش عمق چیست؟ فرض کنید من در حال حاضر روی یک ربات زیر آب کار می کنم و امیدوار هستم که از حباب های گاز تولید شده توسط الکترولیز آب برای کنترل شناوری استفاده کنم. عمق عملیاتی بین 200 تا 1000 متر است.هر چه فشار بیشتر باشد کار را بسیار دشوارتر می کند. ولی...
برای الکترولیز آب به الکترودهایی با پتانسیل زیاد، ترجیحاً بزرگ با فاصله الکترودهای کوچک بین آنها نیاز دارید. شما می خواهید آب شفاف و صاف شده و بدون برق گرفتگی ماهی ها، تمام زیردریایی را به دلیل اتصال کوتاه تصادفی بسوزانید.
و برای کنترل شناوری به گاز زیادی نیاز خواهید داشت، به خصوص در اعماق 200-1000 متر، بنابراین به برق زیادی نیاز دارید:
طبق قانون فارادی
$m=(Q/F)(M/z)$
که در آن $F = 96485\ \mathrm{C/mol}$ می توانید مانند 4.5 لیتر گاز هیدروژن (1 اتمسفر، 25 درجه سانتی گراد) با جریان 10 آمپر در 1 ساعت بسازید! این معادل 0.04 لیتر در 1000 متر (100 اتمسفر) گاز بالقوه انفجار است.
آیا حجم آب درگیر بر سرعت الکترولیز تأثیر می گذارد؟من در حال کار بر روی طراحی یک الکترولیز PEM خانگی هستم و هدف من این است که آن را تا حد امکان فشرده کنم تا امکان حمل و نقل آسان را فراهم کنم. سوال من، همانطور که به آن مربوط می شود، این است که آیا - با همان جریان اعمال شده - حجم آب داخل الکترولیز بر سرعت تجزیه به H2 و O2 تأثیر می گذارد؟عوامل زیادی وجود دارد که بر نرخ تأثیر می گذارد، به عنوان مثال. مساحت، فاصله و نوع الکترودها، الکترولیت، چگالی جریان و جریان، و غیره. اما، اگر تنها عامل تغییر حجم بود (یعنی الکترودها کاملاً غوطه ور هستند و همیشه در بالای محلول روی یک شناور هستند، نه در پایین محلول که فشار وجود دارد. ممکن است تغییر کند)، حجم در ابتدا تأثیری نخواهد داشت.
با این حال، همانطور که واکنش ادامه می یابد و غلظت الکترولیت شروع به تغییر می کند، به دلیل از دست دادن آب و احتمالاً به دلیل انحلال الکترودها، غلظت با حجم زیاد الکترولیت کندتر تغییر می کند. بنابراین، ممکن است یک تفاوت مرتبه دوم با ادامه الکترولیز وجود داشته باشد.
آیا تغییر غلظت الکترولیت در الکترولیز آب بر سرعت تولید گاز هیدروژن در کاتد تأثیر می گذارد؟با کاهش غلظت الکترولیت، یا ولتاژ مورد نیاز در جریان ثابت افزایش می یابد، یا جریان عبوری در ولتاژ ثابت کاهش می یابد.
هر دو به این دلیل اتفاق میافتند که در غلظتهای پایینتر، گرادیان پتانسیل بالاتری در الکترولیت برای حفظ جریان یکسان مورد نیاز است، زیرا تعداد یونهای کوچکتر نیاز به حرکت سریعتر یونها برای همان جریان دارد.
این گرادیان پتانسیل و افت پتانسیل ناشی از آن در برابر ولتاژ خارجی عمل می کند. پتانسیل های الکترود اجباری را به پتانسیل تعادل آنها نزدیک می کند. سپس واکنشهای الکترود خالص کندتر میشوند.
چگونه آنها الکترولیز را در گرانش صفر انجام می دهند؟اساساً، من تصور می کنم که انجام الکترولیز در گرانش صفر دشوار است، زیرا شما اساساً تمام کنترل خود را در مورد جایی که گاز خروجی می رود از دست می دهید. چگونه این را حل می کنند؟من حدس میزنم پاسخ کلی برای هر سیستم جداسازی جرمی این باشد که شما آن را بچرخانید، اما جداسازی جرم واقعاً برای الکترولیز مؤثر نیست، زیرا این جداسازی بیشتر بین آند و کاتد نیاز دارد که منجر به تلفات اهمی پروتونیک، یعنی افزایش مقاومت داخلی میشود. بنابراین جداسازی بهینه گونه ها نه با جرم آنها، بلکه با اندازه و بار آنها، معمولاً از طریق یک غشای تبادل پروتون (PEM) انجام می شود.
الکترولیز PEM امکان قرار دادن الکترود محکمتر را برای کاهش تلفات اهمی فراهم میکند، جریان بالاتری را امکانپذیر میکند و در برابر فشارهای نسبتاً بالا متحمل است. آب اگر از انتهای آند تغذیه شود و با جریان از کاتد به سمت آند، آب به هیدروژن و اکسیژن جدا می شود، هیدروژن با بار مثبت از طریق PEM به سمت کاتد با بار منفی جذب می شود و اکسیژن با بار منفی از کاتد به سمت آند دفع می شود. آند با بار مثبت:

الکترولیز PEM منبع اصلی اکسیژن در ایستگاه فضایی بینالمللی است و از شمعهای پرکلرات به عنوان پشتیبان (برای مواقع اضطراری یا زمانی که دستگاه الکترولیز کار نمیکند) استفاده میکند.
ژنراتور بر اساس یک اصل ساده کار می کند - الکترولیز، تفکیک اکسیژن و هیدروژن از آب از طریق استفاده از برق. چه چیزی ژنراتور را ایمن می کند؟ این دستگاه از یک غشای تبادل پروتون (PEM) برای جداسازی هیدروژن و اکسیژن تولید شده استفاده می کند.
در الکترولایزر PEM، آب در الکترود اکسیژن یا آند سلولی اکسید میشود تا گاز اکسیژن تولید کند و یونهای هیدروژن (پروتون) و الکترونها آزاد شود. یون های هیدروژن از آند سلول به کاتد سلول یا الکترود هیدروژن تحت تأثیر میدان الکتریکی اعمال شده در سراسر سلول مهاجرت می کنند، در حالی که الکترون ها توسط یک منبع برق dc منتقل می شوند. پروتون ها و الکترون ها در کاتد سلول دوباره ترکیب می شوند و هیدروژن تولید می کنند. آب مایع نیز در کاتد به دلیل فرآیندی به نام درگ الکترواسموتیک آزاد می شود. اکسیژن و هیدروژن در یک نسبت استوکیومتری - دو واحد حجمی هیدروژن برای هر یک از اکسیژن - با نرخی متناسب با جریان سلول اعمال شده تولید می شوند.
تولید هیدروژن تحت فشار در زیر آب و سپس استفاده از آن برای انجام کار
همانطور که حدس زدید، این کار نمی کند زیرا الکترولیز آب در فشار بالا دشوارتر است. طبق معادله نرنست، تغییر انرژی آزاد گیبس (و در نتیجه ولتاژ مورد نیاز) برای یک واکنش الکتروشیمیایی به غلظت واکنش دهنده ها و محصولات بستگی دارد. غلظت گاز با فشار جزئی آن اندازه گیری می شود. در این حالت، واکنش در عمق بیشتر نامطلوب تر می شود، زیرا غلظت آب به سختی تغییر می کند در حالی که فشار گازهای محصول (هیدروژن و اکسیژن) افزایش می یابد

-
sohrab 4242
نام: سهراب نعمتی
عضویت : سهشنبه ۱۴۰۱/۹/۸ - ۲۱:۴۷
پست: 11-
- جنسیت:
Re: الکترولیز آب تحت فشار
سلام از یک لیتر آب چقدر میتوان گاز هیدروژن و اکسیژن گرفت به عبارتی گازهای حاصله از یک لیتر چه حجمی را اشغال میکند ممنون
- rohamavation
نام: roham hesami radرهام حسامی راد
محل اقامت: 100 مایلی شمال لندن جاده آیلستون، لستر، لسترشر. LE2
عضویت : سهشنبه ۱۳۹۹/۸/۲۰ - ۰۸:۳۴
پست: 3286-
سپاس: 5494
- جنسیت:
تماس:
Re: الکترولیز آب تحت فشار
من از دبیرستان شیمی نخوندم ولی اونجه ازدرس ترمودینامیک و سوخت احتراق میدونم این هست اگه اشتباه نکنم با توجه به اینکه سرعت جریان سیالات و همچنین حجم مایعات و گازها به شدت به دما و فشار وابسته هستش وجود شرایط مرجع استاندارد، در محاسبات اهمیت بسیاری داره از شرایط STP زمانی استفاده میشود که «شرایط حالت استاندارد» (Standard State Conditions) را در محاسبات بکار ببریم.حجم یک نمونه شامل 1/4 مول گاز هیدروژن (H2) را در شرایط STP محاسبه کنید.
با توجه به تعریف شرایط STP میدانیم که دما و فشار به ترتیب برابر با 273/15 کلوین و ۱ اتمسفر است. مقدار ثابت جهانی گازها (R) نیز برابر با 0/08206 در نظر گرفته میشه. با جایگذاری مقادیر در قانون گازهای ایدهآل،:$(1 \mathrm{atm})(\mathrm{V})=(1.4 \mathrm{mol})(0.08206)(273.15 \mathrm{K})=31.4 \mathrm{L}$
در نتیجه، میبینیم که 1/4 مول از گاز هیدروژن، حجم 31/4 لیتر را اشغال میکنه
با فرض شرایط STP، میتوان معادله گازهای ایدهآل را سادهتر کرد. درحقیقت با فرض P=1 و T=273.15 و بازآرایی رابطه برای محاسبه حجم، به رابطه زیر میرسم V=nR(273.15)از رابطه بالا میتوانیم برای محسابه حجم مولی یک گاز در شرایط STP استفاده کنیم. در نتیجه، با قراردادن n=1
در معادله دارم V=R(273.15)≈22.4L
در یک لیتر آب حدود 111.11 گرم هیدروژن با حجم 1.33 متر مکعب و 888.8 گرم اکسیژن و حجم آن 0.670 متر مکعب است جرم مولی آب = 18 گرم، که H2 = 2 گرم، O = 16 گرم. بنابراین 2/18 = 1/9 = 11%.بنابراین یک لیتر آب 110 گرم گاز هیدروژن می دهد که در دما و فشار معمولی حدود 1.3 متر مکعب گاز است.
هیدروژن و اکسیژن را می توان با هیدرولیز از آب جدا کرد یا تولید کرد. معادله متعادل این واکنش به صورت زیر است:
2 H2O → 2H2 + O2
می توانید نتیجه بگیرید که 1 مول H2O 1 مول H2 تولید می کند
اکنون 1.0 لیتر آب مصرف می کنید. چگالی آب در 25 درجه سانتیگراد = 997 گرم در لیتر
مول آب در 997 گرم:
جرم مولی آب = 2*1.008 + 15.999 = 18.015 گرم بر مول
مول H2O در 997 گرم = 997 گرم / 18.015 گرم بر مول = 55.34 مول H2O
این 55.34 مول H2 تولید می کند
جرم مولی H2 = 1.008 * 2 = 2.016 گرم
جرم H2 تولید شده = 55.34 مول * 2.016 گرم بر مول = 111.57 گرم یا 0.11157 کیلوگرم
حجم گازهای تولید شده در الکترولیز آب چقدر است
این واکنش است:
$\ce{H_2O(l)->H_2(g) + 1/2 O_2(g)}$
به عنوان یک قانون کلی، در شرایط آزمایشگاهی معمولی (دمای اتاق، فشار 1 اتمسفر)، گازها 1000 برابر حجم مایعات را اشغال می کنند. و از آنجایی که ما در حال ایجاد 1.5 مولکول گاز برای هر مولکول مایع هستیم، افزایش حجم مورد انتظار ما 1500 x است.
حالا بیایید محاسبه رسمی را برای تعیین افزایش واقعی انجام دهیم:
آب مایع چگالی = 1 گرم در میلی لیتر => حجم ویژه آب مایع = 1 میلی لیتر در گرم.
1 مول آب = 18 گرم => حجم 1 مول آب مایع = 18 میلی لیتر = 0.018 لیتر.
حجم 1 مول گاز در 1 اتمسفر، 23 درجه سانتیگراد:
$V = \frac{n R T}{p} = \frac{1 mole \circ 0.082 \frac{L atm}{mol K} \circ (23+273) K}{1 atm} = 24.3 L$
از آنجایی که 1 مول آب مایع به 1.5 مول گاز تجزیه می شود:
حجم 1.5 مول گاز در 1 اتمسفر، 23 C = 24.3 L x 1.5 = 36.5 L
در نهایت، نسبت حجم برابر است با:
$\frac{36.5 L}{0.018 L } = 2030 \simeq 2000$
بنابراین الکترولیز کامل آب مایع در 1 اتمسفر و 23 درجه سانتیگراد حجم آن را 2000 برابر میکنه
در الکترولیز آب چه مقدار هیدروژن یا اکسیژن تولید می شود؟$n = \frac{Q}{Fz}$
در جایی که Q بار عبور داده شده است، F ثابت فارادی و z تعداد الکترون های منتقل شده در هر واکنش ردوکس است. به عنوان مثال، z=2 برای هیدروژن زیرا برای تبدیل H+ به H2 به دو الکترون نیاز است تا $\ce{2H+ + 2e- <=> H2}$. بنابراین، به ازای هر کولن شارژ، دریافت می کنیم:
$\begin{align}
n &= \frac{1\ \mathrm{C}}{(96.485\ \mathrm{kC/mol})(2)}\\
&= 5.18\ \mathrm{µmol}
\end{align}$
گاز هیدروژن تولید شده بنابراین اگر بتوانیم شارژ (یا جریان یکپارچه در طول زمان) را اندازه گیری کنیم، می توانیم مقدار محصول تولید شده را محاسبه کنیم. این بدون توجه به ولتاژ اعمال شده یا محتوای الکترولیت محلول درسته
با توجه به تعریف شرایط STP میدانیم که دما و فشار به ترتیب برابر با 273/15 کلوین و ۱ اتمسفر است. مقدار ثابت جهانی گازها (R) نیز برابر با 0/08206 در نظر گرفته میشه. با جایگذاری مقادیر در قانون گازهای ایدهآل،:$(1 \mathrm{atm})(\mathrm{V})=(1.4 \mathrm{mol})(0.08206)(273.15 \mathrm{K})=31.4 \mathrm{L}$
در نتیجه، میبینیم که 1/4 مول از گاز هیدروژن، حجم 31/4 لیتر را اشغال میکنه
با فرض شرایط STP، میتوان معادله گازهای ایدهآل را سادهتر کرد. درحقیقت با فرض P=1 و T=273.15 و بازآرایی رابطه برای محاسبه حجم، به رابطه زیر میرسم V=nR(273.15)از رابطه بالا میتوانیم برای محسابه حجم مولی یک گاز در شرایط STP استفاده کنیم. در نتیجه، با قراردادن n=1
در معادله دارم V=R(273.15)≈22.4L
در یک لیتر آب حدود 111.11 گرم هیدروژن با حجم 1.33 متر مکعب و 888.8 گرم اکسیژن و حجم آن 0.670 متر مکعب است جرم مولی آب = 18 گرم، که H2 = 2 گرم، O = 16 گرم. بنابراین 2/18 = 1/9 = 11%.بنابراین یک لیتر آب 110 گرم گاز هیدروژن می دهد که در دما و فشار معمولی حدود 1.3 متر مکعب گاز است.
هیدروژن و اکسیژن را می توان با هیدرولیز از آب جدا کرد یا تولید کرد. معادله متعادل این واکنش به صورت زیر است:
2 H2O → 2H2 + O2
می توانید نتیجه بگیرید که 1 مول H2O 1 مول H2 تولید می کند
اکنون 1.0 لیتر آب مصرف می کنید. چگالی آب در 25 درجه سانتیگراد = 997 گرم در لیتر
مول آب در 997 گرم:
جرم مولی آب = 2*1.008 + 15.999 = 18.015 گرم بر مول
مول H2O در 997 گرم = 997 گرم / 18.015 گرم بر مول = 55.34 مول H2O
این 55.34 مول H2 تولید می کند
جرم مولی H2 = 1.008 * 2 = 2.016 گرم
جرم H2 تولید شده = 55.34 مول * 2.016 گرم بر مول = 111.57 گرم یا 0.11157 کیلوگرم
حجم گازهای تولید شده در الکترولیز آب چقدر است
این واکنش است:
$\ce{H_2O(l)->H_2(g) + 1/2 O_2(g)}$
به عنوان یک قانون کلی، در شرایط آزمایشگاهی معمولی (دمای اتاق، فشار 1 اتمسفر)، گازها 1000 برابر حجم مایعات را اشغال می کنند. و از آنجایی که ما در حال ایجاد 1.5 مولکول گاز برای هر مولکول مایع هستیم، افزایش حجم مورد انتظار ما 1500 x است.
حالا بیایید محاسبه رسمی را برای تعیین افزایش واقعی انجام دهیم:
آب مایع چگالی = 1 گرم در میلی لیتر => حجم ویژه آب مایع = 1 میلی لیتر در گرم.
1 مول آب = 18 گرم => حجم 1 مول آب مایع = 18 میلی لیتر = 0.018 لیتر.
حجم 1 مول گاز در 1 اتمسفر، 23 درجه سانتیگراد:
$V = \frac{n R T}{p} = \frac{1 mole \circ 0.082 \frac{L atm}{mol K} \circ (23+273) K}{1 atm} = 24.3 L$
از آنجایی که 1 مول آب مایع به 1.5 مول گاز تجزیه می شود:
حجم 1.5 مول گاز در 1 اتمسفر، 23 C = 24.3 L x 1.5 = 36.5 L
در نهایت، نسبت حجم برابر است با:
$\frac{36.5 L}{0.018 L } = 2030 \simeq 2000$
بنابراین الکترولیز کامل آب مایع در 1 اتمسفر و 23 درجه سانتیگراد حجم آن را 2000 برابر میکنه
در الکترولیز آب چه مقدار هیدروژن یا اکسیژن تولید می شود؟$n = \frac{Q}{Fz}$
در جایی که Q بار عبور داده شده است، F ثابت فارادی و z تعداد الکترون های منتقل شده در هر واکنش ردوکس است. به عنوان مثال، z=2 برای هیدروژن زیرا برای تبدیل H+ به H2 به دو الکترون نیاز است تا $\ce{2H+ + 2e- <=> H2}$. بنابراین، به ازای هر کولن شارژ، دریافت می کنیم:
$\begin{align}
n &= \frac{1\ \mathrm{C}}{(96.485\ \mathrm{kC/mol})(2)}\\
&= 5.18\ \mathrm{µmol}
\end{align}$
گاز هیدروژن تولید شده بنابراین اگر بتوانیم شارژ (یا جریان یکپارچه در طول زمان) را اندازه گیری کنیم، می توانیم مقدار محصول تولید شده را محاسبه کنیم. این بدون توجه به ولتاژ اعمال شده یا محتوای الکترولیت محلول درسته

-
sohrab 4242
نام: سهراب نعمتی
عضویت : سهشنبه ۱۴۰۱/۹/۸ - ۲۱:۴۷
پست: 11-
- جنسیت:
Re: الکترولیز آب تحت فشار
آیا با فشار حاصله از انباشته شدن گازها درالکترولیز میتوان آب را به ارتفاع پمپاژ کرد
- rohamavation
نام: roham hesami radرهام حسامی راد
محل اقامت: 100 مایلی شمال لندن جاده آیلستون، لستر، لسترشر. LE2
عضویت : سهشنبه ۱۳۹۹/۸/۲۰ - ۰۸:۳۴
پست: 3286-
سپاس: 5494
- جنسیت:
تماس:
Re: الکترولیز آب تحت فشار
در یک دستگاه الکترولیز بسته فشار می تواند بسیار زیاد بشه (شما می توانید حد تئوری را با استفاده از قانون گاز ایده آل و چگالی آب محاسبه کنید.بهتره بگی از الکترولیز آب چه فشاری ایجاد می شود؟هدف من این است که مقادیر کمی H2 و O2 ایزوله برای یک مشعل هیدروژنی سرگرمی بسازم و کنجکاو هستم که چگونه می توانم شاخه میانی ولتامتر هافمن را قبل از اینکه فشار برگشتی تولید گاز جدید را متوقف کنه بلند کنم. داشتن فشار گاز قابل پیش بینی به من این امکان را میده که از فضاهای جمع آوری برای ذخیره گاز استفاده کنم..یک دستگاه الکترولیز هافمن دو گاز را به طور جداگانه جمع آوری میکنه و نسبت 2 به 1 را به خوبی نشان می دهد.ولتامتر هافمن برای نشان دادن ترکیب شیمیایی آب بر حسب حجم و معادل الکتروشیمیایی هیدروژن با الکترولیز آب استفاده میشه
چه پارامترهایی به احتمال زیاد بر این فشار، ترکیب الکترولیت، دما، ولتاژ تأثیر میزارن
آیا انتظار می رود فشار H2 و O2 در تئوری و/یا عمل یکسان باشد؟
به نظر می رسد که یک فرآیند الکترولیز فشار بالا وجود دارد که در بسیاری از اتمسفرهای فشار عمل میکنه و برای تحت فشار قرار دادن محصولات گازی استفاده میشه اگرچه اطلاعات من محدوده به نظر میرسه این یک فرآیند تخصصی است که معمولاً با سیستمهای غشای تبادل پروتون مرتبط است، فکر میکنم، اما من فقط امیدوار هستم که از دو الکترود فلزی استفاده کنم.حداکثر فشار گازی که می توانید در ولتامتر هافمن انتظار داشته باشید، فشار اتمسفر به اضافه فشار ستون آب در سیلندر میانی (1 atm/10m) است.
برای یک دستگاه با اندازه معقول، شما به شرایطی نخواهید رسید که مجبور باشید اثرات "فشار برگشتی" را در نظر بگیرین که ممکن است تولید هیدروژن یا اکسیژن را متوقف کنه
با توجه به اینکه سطح مقطع هر سه سیلندر یکسان است، فشار هیدروژن کمی بیشتر از فشار اکسیژن است زیرا ستون آبی که فشار را اضافه می کند بیشتر است ک نقطه نگرانی تولید هیدروژن تحت فشار زیاد.
تحت فشار فزاینده، هم هیدروژن و هم اکسیژن به طور فزاینده ای در آب پخش میشن سپس به ستون های مقابل، و از مخلوط شدن با گازهای ستون دیگر جلوگیری می کنند.
در واقع، حتی در فشارهای پایین، با توجه به زمان کافی، انتشار باعث اختلاط گازها می شود. خلوص نسبی هم به میزان تولید و هم به سرعت انتشار مربوط میشه
چه پارامترهایی به احتمال زیاد بر این فشار، ترکیب الکترولیت، دما، ولتاژ تأثیر میزارن
آیا انتظار می رود فشار H2 و O2 در تئوری و/یا عمل یکسان باشد؟
به نظر می رسد که یک فرآیند الکترولیز فشار بالا وجود دارد که در بسیاری از اتمسفرهای فشار عمل میکنه و برای تحت فشار قرار دادن محصولات گازی استفاده میشه اگرچه اطلاعات من محدوده به نظر میرسه این یک فرآیند تخصصی است که معمولاً با سیستمهای غشای تبادل پروتون مرتبط است، فکر میکنم، اما من فقط امیدوار هستم که از دو الکترود فلزی استفاده کنم.حداکثر فشار گازی که می توانید در ولتامتر هافمن انتظار داشته باشید، فشار اتمسفر به اضافه فشار ستون آب در سیلندر میانی (1 atm/10m) است.
برای یک دستگاه با اندازه معقول، شما به شرایطی نخواهید رسید که مجبور باشید اثرات "فشار برگشتی" را در نظر بگیرین که ممکن است تولید هیدروژن یا اکسیژن را متوقف کنه
با توجه به اینکه سطح مقطع هر سه سیلندر یکسان است، فشار هیدروژن کمی بیشتر از فشار اکسیژن است زیرا ستون آبی که فشار را اضافه می کند بیشتر است ک نقطه نگرانی تولید هیدروژن تحت فشار زیاد.
تحت فشار فزاینده، هم هیدروژن و هم اکسیژن به طور فزاینده ای در آب پخش میشن سپس به ستون های مقابل، و از مخلوط شدن با گازهای ستون دیگر جلوگیری می کنند.
در واقع، حتی در فشارهای پایین، با توجه به زمان کافی، انتشار باعث اختلاط گازها می شود. خلوص نسبی هم به میزان تولید و هم به سرعت انتشار مربوط میشه

-
sohrab 4242
نام: سهراب نعمتی
عضویت : سهشنبه ۱۴۰۱/۹/۸ - ۲۱:۴۷
پست: 11-
- جنسیت:
Re: الکترولیز آب تحت فشار
ما میتوانیم فشار داخل یک مخزن را آنقدر بالا ببریم تا حدی که مخزن منفجر شود با بخار آب و جوشاندن آیا این کار را با عمل الکترولیز هم. میتوانیم انجام دهیم الکترولیز قدرت بخار را دارد
- rohamavation
نام: roham hesami radرهام حسامی راد
محل اقامت: 100 مایلی شمال لندن جاده آیلستون، لستر، لسترشر. LE2
عضویت : سهشنبه ۱۳۹۹/۸/۲۰ - ۰۸:۳۴
پست: 3286-
سپاس: 5494
- جنسیت:
تماس:
Re: الکترولیز آب تحت فشار
من قبل هم بهتون گفتم .با افزایش پرشر، راندمان الکترولیز به طور کلی کاهش پیدا میکنه اما در لو پرشر (از 1 اتمسفر به 5 اتمسفر) و چگالی جریان بالا افزایش می یابه خوب بازم اگر شما تو این مخزن میخواین انجام بدین خوب بسته به پرشر و دما و جریان ورودی داره اگه میخواین گازها رو استخراج بعد تو یک مخزن دیگه تحت پرشر قرار بدین خوب اره حق با شماست .میتونید ولی اگه میخواین گازها رو میکسچر کنی بعد اب تولی کنید بحث اون جداست.
واکنش واقعی برای تولید آب کمی پیچیده تره:$$\ce{2H2_{(g)} + O2_{(g)} -> 2H2O_{(g)} + energy}$$ برای تولید دو مولکول آب (H2O)، دو مولکول هیدروژن دو اتمی (H2) باید با یک مولکول اکسیژن دو اتمی (O2) ترکیب بشن انرژی در این فرآیند آزاد میشه
وقتی هیدروژن و اکسیژن را با هم مخلوط می کنیم چه اتفاقی میفته
هیدروژن با اکسیژن با هم میکسچر میشن و یک اکسپلوسیو میکسچر میده. از آنجایی که هیدروژن و اکسیژن قبل از وقوع اکسپلوژن باید با هم مخلوط شوند، اکسپلوژن نسبتا آهسته و پراکنده هست.برای ایجاد آب، اتم های اکسیژن و هیدروژن باید وجود داشته باشن
صرف میکسچر کردن آنها با هم کمکی به شما نمی کنه . شما هنوز با اتم های هیدروژن و اکسیژن مجزا باقی موندین. مدارهای الکترون های هر اتم باید به هم متصل شوند و برای انجام این کار باید یک انفجار ناگهانی انرژی داشته باشیم تا این چیزها به هم متصل شوند.
بررسی ویژگیهای انفجار مخلوطهای هیدروژن-هوا و هیدروژن-اکسیژن در های پرشر بالا شامل دادههایی برای پرشر تا 200 بار است.
داده ها برای مخلوط های هیدروژن-اکسیژن در هر دو دمای 20 و 80 درجه سانتیگراد در پرشر های 1 تا 200 بار جمع آوری شد. یک جرقه ولتاژ بالا هنوز برای ایجاد انفجار لازم بود.
ذخیره سازی مخلوط فشرده هیدروژن و اکسیژن هنوز برای من بسیار ناامن به نظر می رسد. قطعا این کار را نمی کنم
در واقع به آن می گویند احتراق! وقتی گاز هیدروژن و اکسیژن را می سوزانید، واکنش به این صورت است:
$\ce{2H2_{(g)} + O2_{(g)} -> 2H2O_{(g)} + energy}$
اساساً، شاتل فضایی سابق ایالات متحده را میتوان به عنوان یک ماشین بزرگ دید که هیدروژن و اکسیژن را به آب تبدیل میکند. (توجه: شاتل فضایی از هیدروژن و اکسیژن مایع استفاده کرده است، اما در غیر این صورت اصل و فرمول دقیقاً یکسان است)
از آنجایی که انرژی آزاد گیبس در واکنش رو به جلو منفی است (-242 کیلوژول بر مول)، شما نیازی به اضافه کردن انرژی به سیستم ندارید، واکنش خود به خود است (به خاطر داشته باش شما عموماً به اسپارک نیاز دارید تاکمباسشن را مشتعل کند، زیرا اسپارک وجود داره یک مانع جنبشی برای واکنش به نام انرژی فعال سازی).البتهالبته در عمل برای تولید گرمای خروجی لازم، موتور شاتل باید بخش زیادی از سوخت هیدروژن خود را با استفاده از اکسیژن حمل شده در قسمت دیگری از مخزن خارجی خود بسوزانه از واکنش هیدروژن و اکسیژن، آب تولید می شود که هر مولکول آن حدود 18 برابر سنگین تر از یک مولکول هیدروژنه. ابر سفید عظیمی که در هنگام انفجار چلنجر در آسمان دیده شد تقریباً به طور کامل بخار آب متراکم شده بود، نه دود.
واکنش معکوس آب به هیدروژن و اکسیژن، دارای انرژی آزاد گیبس مثبت است، بنابراین برای انجام واکنش باید انرژی را به شکل الکتریسیته به سیستم اضافه کنید امیدورارم دیگه کامل مطلب گرفته باشید
واکنش واقعی برای تولید آب کمی پیچیده تره:$$\ce{2H2_{(g)} + O2_{(g)} -> 2H2O_{(g)} + energy}$$ برای تولید دو مولکول آب (H2O)، دو مولکول هیدروژن دو اتمی (H2) باید با یک مولکول اکسیژن دو اتمی (O2) ترکیب بشن انرژی در این فرآیند آزاد میشه
وقتی هیدروژن و اکسیژن را با هم مخلوط می کنیم چه اتفاقی میفته
هیدروژن با اکسیژن با هم میکسچر میشن و یک اکسپلوسیو میکسچر میده. از آنجایی که هیدروژن و اکسیژن قبل از وقوع اکسپلوژن باید با هم مخلوط شوند، اکسپلوژن نسبتا آهسته و پراکنده هست.برای ایجاد آب، اتم های اکسیژن و هیدروژن باید وجود داشته باشن
صرف میکسچر کردن آنها با هم کمکی به شما نمی کنه . شما هنوز با اتم های هیدروژن و اکسیژن مجزا باقی موندین. مدارهای الکترون های هر اتم باید به هم متصل شوند و برای انجام این کار باید یک انفجار ناگهانی انرژی داشته باشیم تا این چیزها به هم متصل شوند.
بررسی ویژگیهای انفجار مخلوطهای هیدروژن-هوا و هیدروژن-اکسیژن در های پرشر بالا شامل دادههایی برای پرشر تا 200 بار است.
داده ها برای مخلوط های هیدروژن-اکسیژن در هر دو دمای 20 و 80 درجه سانتیگراد در پرشر های 1 تا 200 بار جمع آوری شد. یک جرقه ولتاژ بالا هنوز برای ایجاد انفجار لازم بود.
ذخیره سازی مخلوط فشرده هیدروژن و اکسیژن هنوز برای من بسیار ناامن به نظر می رسد. قطعا این کار را نمی کنم
در واقع به آن می گویند احتراق! وقتی گاز هیدروژن و اکسیژن را می سوزانید، واکنش به این صورت است:
$\ce{2H2_{(g)} + O2_{(g)} -> 2H2O_{(g)} + energy}$
اساساً، شاتل فضایی سابق ایالات متحده را میتوان به عنوان یک ماشین بزرگ دید که هیدروژن و اکسیژن را به آب تبدیل میکند. (توجه: شاتل فضایی از هیدروژن و اکسیژن مایع استفاده کرده است، اما در غیر این صورت اصل و فرمول دقیقاً یکسان است)
از آنجایی که انرژی آزاد گیبس در واکنش رو به جلو منفی است (-242 کیلوژول بر مول)، شما نیازی به اضافه کردن انرژی به سیستم ندارید، واکنش خود به خود است (به خاطر داشته باش شما عموماً به اسپارک نیاز دارید تاکمباسشن را مشتعل کند، زیرا اسپارک وجود داره یک مانع جنبشی برای واکنش به نام انرژی فعال سازی).البتهالبته در عمل برای تولید گرمای خروجی لازم، موتور شاتل باید بخش زیادی از سوخت هیدروژن خود را با استفاده از اکسیژن حمل شده در قسمت دیگری از مخزن خارجی خود بسوزانه از واکنش هیدروژن و اکسیژن، آب تولید می شود که هر مولکول آن حدود 18 برابر سنگین تر از یک مولکول هیدروژنه. ابر سفید عظیمی که در هنگام انفجار چلنجر در آسمان دیده شد تقریباً به طور کامل بخار آب متراکم شده بود، نه دود.
واکنش معکوس آب به هیدروژن و اکسیژن، دارای انرژی آزاد گیبس مثبت است، بنابراین برای انجام واکنش باید انرژی را به شکل الکتریسیته به سیستم اضافه کنید امیدورارم دیگه کامل مطلب گرفته باشید

-
sohrab 4242
نام: سهراب نعمتی
عضویت : سهشنبه ۱۴۰۱/۹/۸ - ۲۱:۴۷
پست: 11-
- جنسیت:
Re: الکترولیز آب تحت فشار
سلام به اساتید محترم از مجموع جواب داده شده به این نتیجه میرسیم که انباشته شدن گازها درالکترولیز بصورت مخلوط و فشرده خطرناک است اگر اینها جدا از هم انباشته و فشرده سازی کنیم چطور باز هم خطر دارد تا چه فشاری خطر ندارد ممنون از اینکه وقت گذاشتید
- rohamavation
نام: roham hesami radرهام حسامی راد
محل اقامت: 100 مایلی شمال لندن جاده آیلستون، لستر، لسترشر. LE2
عضویت : سهشنبه ۱۳۹۹/۸/۲۰ - ۰۸:۳۴
پست: 3286-
سپاس: 5494
- جنسیت:
تماس:
Re: الکترولیز آب تحت فشار
ببین به مخزن شما بستگی داره گفتم تا جرقه نباشه هرگز انفجاری نداری به عوامل زیادی مثل جنس دیواره دما فشار استرس Toughness.محاسبه وضعیت استرس بین چقرمگی شکست ضریب شدّت تنش بحرانی یک ترک تیز که در آن، انتشار ترک بهطور ناگهانی سریع و نامحدود میشود. مقدار بحرانی ضریب شدّت تنش در حالت بارگذاری mode I که تحت شرایط کرنش صفحهای اندازهگیری میشود، به عنوان چقرمگی شکست کرنش صفحهای شناخته شده و با$ {\displaystyle K_{\text{Ic}}}$ میگیم چقرمگی شکست یک روش کمّی برای بیان مقاومت یک ماده نسبت به انتشار ترک برای یک ماده ی خاص است.چقرمگی را می توان با ادغام منحنی تنش-کرنش تعیین کرد. [1] انرژی تغییر شکل مکانیکی در واحد حجم قبل از شکست است.${\displaystyle {\tfrac {\mbox{energy}}{\mbox{volume}}}=\int _{0}^{\varepsilon _{f}}\sigma \,d\varepsilon }$اگر حد بالایی ادغام تا نقطه تسلیم محدود شود، انرژی جذب شده در واحد حجم به عنوان مدول ارتجاعی شناخته می شود. از نظر ریاضی، مدول تاب آوری را می توان با حاصل ضرب مجذور تنش تسلیم تقسیم بر دو برابر مدول کشش یانگ بیان کرد. به این معنا که مدول تاب آوری =تنش تسلیم 2/
2 (مدول یانگ) چقرمگی = توانایی یک ماده برای جذب انرژی بدون شکست. در منحنی تنش-کرنش، ناحیه زیر منحنی اغلب معیاری برای چقرمگی در نظر گرفته می شود. در طرح زیر، ماده 2 چقرمگی بالاتری نسبت به ماده 1 دارد. (من باید آنها را به گونه ای طراحی می کردم که به وضوح متفاوت باشند، اما فرض کنید مساحت زیر منحنی ماده 2 بیشتر از مساحت زیر منحنی ماده 1 باشد.) بنابراین، ماده 2 ممکن است استحکام کمتری نسبت به ماده 1 داشته باشد اما می تواند انرژی کل بیشتری را قبل از شکست جذب کند.
سختی = توانایی یک ماده برای مقاومت در برابر تغییر شکل پلاستیک.
توجه داشته باشید که طرح دو منحنی ماده فرضی (خیالی) را منعکس می کند. بسیاری دیگر از پروفایل های منحنی تنش-کرنش امکان پذیر است. همچنین توجه داشته باشید که شرح چقرمگی ارائه شده در اینجا بر اساس چقرمگی مواد کلی است که تنها یک راه برای ارزیابی چقرمگی است. چقرمگی ضربه، چقرمگی بریدگی و چقرمگی شکست نیز وجود داره
ابتدا باید فشار دیوارها را محاسبه کنید. برای انجام این کار، یک صفحه برش را در هر قطری از ظرف تصور کنید. اکنون، نیروها را روی نیمی از کشتی متعادل کنید. در یک جهت، نیروی فشار سیال را دارید که مجموعاً به$F = \pi R^2 P$ می رسه. در جهت دیگر، تنها نیروی متعادل کننده، تنش در دیوارها است که بر روی سطح مقطع در معرض قرار می گیرند. نیرو در اینجا برابر است با $F = 2\pi R t \sigma_{wall}$، که t ضخامت دیوار است. با برابر قرار دادن این نیروها، می توانیم محاسبه کنیم که تنش در دیوار است
$\sigma_{wall} = \frac{P R}{2t}.$
حال به دلیل تقارن مسئله، و ساده سازی (معتبر) تنش ضخامت صفر، می توانیم حالت تنش کامل هر نقطه از دیوار را بنویسیم:
$\mathbf{\sigma} = \sigma_{wall}
\left(
\mathbf{e}_{\theta}
\otimes
\mathbf{e}_{\theta}
+
\mathbf{e}_{\phi}
\otimes
\mathbf{e}_{\phi}
\right)
+
0\;
(\mathbf{e}_{r}
\otimes
\mathbf{e}_{r})$
معیار بازده را بررسی کنم
برای محاسبه نقطه ای که تسلیم اتفاق می افتد، باید تنش کششی معادل میزس را محاسبه کنید. تعاریف معادل مختلفی وجود دارد، اما همه شما را به این نتیجه می رساند که برای جلوگیری از تغییر شکل پلاستیک، $\sigma_{wall} < \sigma_y$ که σy تنش تسلیم کششی تک محوری ماده است. بنابراین، حداکثر فشاری که ظرف می تواند قبل از تسلیم داشته باشد، است
$P < \frac{2\,t\,\sigma_{y}}{R}$
هنوز باید شکستگی را در نظر بگیرید، اما این یک بحث جداگانه است که بیشتر برای کلاس مهندسی مناسب است. (اگر این همان چیزی است که به دنبال آن هستید، می توانم به آنجا بروم...) با این معیار، معیار "نشتی قبل از شکست" وجود دارد که یک کران بالایی (غیر شهودی، اما بررسی می کند) روی ضخامت ایمن قرار می دهد. دیواره های رگ
نکته دیگری که باید در نظر داشت این است که فشار در مخزن با دما تغییر می کند. مطمئن شوید که این را در تجزیه و تحلیل خود با $PV = nRT$ یا یک معادله حالت مناسب دیگر در نظر بگیرید.
چگونه حداکثر فشاری که یک ظرف می تواند تحمل کند را محاسبه کنم؟در ابتدا، برای حل حداکثر فشاری که یک ظرف معین می تواند تحمل کند، فکر کردم که شاید بتوانم از مدول یانگ استفاده کنم، که تنش روی یک جسم را به فشاری که توسط یک جسم احساس می شود مرتبط می کند. تغییر در "طول" کره با در نظر گرفتن تغییر شعاع کره به مقدار کمی و دیدن اینکه چه اتفاقی برای یک عنصر کوچک افتاد (به هر حال این برنامه من بود) به دست میآورم. سپس متوجه شدم که از آنجایی که نیروی وارد شده به جسم واقعاً در جهت کشش نیست، بلکه عمود بر آن است
استحکام کششی نهایی وجود دارد! استحکام کششی نهایی بر حسب واحد فشار داده می شود، بنابراین فکر کردم که شاید پاسخ سوال من فقط عدد ذکر شده در مقاله ویکی پدیا باشد. این نه تنها به شدت رضایت بخش نبود، بلکه اشتباه به نظر می رسد، زیرا به نظر می رسد استحکام کششی نهایی دلالت بر این دارد که نیروی کشش در همان جهت کشش باشد. مدتی است که هیچ ایده خوبی به من نرسیده است، بنابراین فکر کردم باید بپرسم، چگونه حداکثر فشاری که یک ظرف معین می تواند داشته باشد را محاسبه کنم؟
مفهوم: استرس حلقه تنشی است که در طول محیط هنگام اعمال فشار ایجاد می شود. تنش حلقه عمود بر جهت محوری عمل می کند. تنش های حلقه ای کششی هستند و برای مقاومت در برابر اثر ترکیدن ناشی از اعمال فشار ایجاد می شوند.تنش در مخازن استوانهای
مطابق با شکل زیر مخزنی استوانهای را در نظر بگیرید. فرض کنید این مخزن حاوی گازی با فشار p است. مطابق با شکل زیر قطر و ضخامت این مخزن به ترتیب برابر با D و t و طول آن برابر با L در نظر گرفته شدهاند. برای بدست آوردن تنش مماسی، مخزن مطابق با شکل زیر برش زده میشود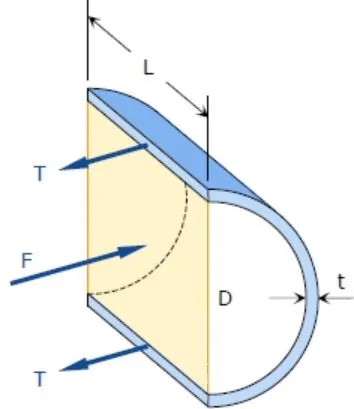
پوسته آبی رنگ در تعادل است؛ بنابراین نیروی ناشی از فشارِ p با نیروی ناشی از تنش مماسی برابر است. در نتیجه با نوشتن رابطه تعادل داریم:
$\Large 2 T = F$
از طرفی نیروی T برابر با حاصل ضرب تنشِ σt در مساحتِ tL است. بنابراین رابطه فوق را میتوان به صورت زیر بازنویسی کرد.
$\Large 2 ( \sigma _ t t L ) = p D L$
نهایتا تنش مماسی در یک مخزن جدار نازکِ استوانهای با فشار p برابر با مقدار زیر بدست میآید.
$\Large 2 t \sigma _ t = p D$
رابطه ۱$\Large \boxed {\sigma_t = \dfrac { p D } { 2 t } }$
برای بدست آوردن تنش طولی کافی است تا مخزن استوانهای مطابق با شکل زیر، به صورت عمود به طول استوانه برش زده شود.
تنش در مخازن
نیروی وارد به انتهای استوانه برابر است با:$\Large F = p A = p \dfrac { \pi} {4} D ^2$
از طرفی تنش طولی تنها روی بخش جدار نازک اعمال میشود. مساحت این قسمت برابر با
$\large A = \pi D t$
است. از این رو نیروی ناشی از تنش طولی نیز برابر است با:
$\Large P _ T = \sigma _ L \pi D t$
در مرحله بعد معادله تعادل نیرویی را به صورت زیر بیان میکنیم.
$\Large \Sigma F _ H = 0$و$\Large P_T = F$و$\Large \sigma _ L \, \pi D t = p \dfrac {\pi} { 4 } D ^ 2$
نهایتا تنش طولی به صورت زیر بدست میآید.
$\Large \boxed {\sigma_t = \dfrac { p D } { 2 t } }$
توجه داشته باشید در روابط فوق منظور از فشار، در حقیقت اختلاف فشار داخل و بیرونِ مخزن است. بنابراین با فرض این که فشار داخلی برابر با pi و فشار خارجی برابر با po باشد، رابطه زیر را میتوان برای تنش طولی بیان کرد.$\Large F = p A = p \dfrac { \pi} {4} D ^2$
با توجه به روابط ۱ و ۲، رابطه زیر را میتوان بین تنشهای افقی و عمودی نوشت.
$\Large \sigma _ t = 2 \sigma _ L$
تنش در مخازن کروی
به دلیل متقارن بودن شکل کره نسبت به تمامی محورهایی که از مرکز آن عبور میکنند، تنش در پوسته یک مخزن کروی، در تمامی جهات با هم برابر هستند. از این رو به منظور محاسبه تنش، تنها کافی است تا مطابق با شکل زیر، کره را در جهتی دلخواه برش بزنید.
تنش در مخازن
نیروی داخلیِ ناشی از فشار که به نیمکره وارد میشود، برابر است با:
$\Large P = p ( \frac { 1 } { 4 } \pi D ^ 2 )$
این نیرو برابر با تنشی است که به جداره وارد میشود. بنابراین میتوان گفت:
$\Large P_T = F$
$\Large \sigma \pi D t = p (\frac {1}{4} \pi D ^ 2)$
نهایتا تنش در جداره یک مخزن کروی با فشار p برابر است با:
$\Large \boxed { \sigma = \dfrac { p D } { 4 t } }$
نحوه محاسبه مقاومت فشار خارجی سیلندرها و کره ها
اگر دیواره های مخزن به اندازه کافی نازک باشد، تحت فشار خارجی نه به دلیل رسیدن مواد به نقطه تسلیم، بلکه به دلیل ناپایداری (کمانش) از بین می رود. به عنوان مثال، یک فشار بحرانی برای یک استوانه بی نهایت جدار نازک با شکل کامل $p=\frac{2 E}{1-\mu^2}(t/D)^3$ است، که در آن E مدول الاستیسیته، μ نسبت پواسون، t ضخامت دیواره و D قطر سیلندر است
حداقل ضخامت یک مخزن تحت فشار سیلندر بیضویبرای مخازن تحت فشار به شکل استوانههای دایرهای، میتوانیم از σhoop=prt استفاده کنیم تا حداقل ضخامت پوست را با تنظیم تنش حلقه حداکثر مقدار مجاز و سپس حل کردن t استفاده کنیم. اما، سیلندرهای بیضوی (پیچیده تر) چطور؟
از آنجایی که بیضی ها دارای یک محور نیمه اصلی و یک محور نیمه فرعی هستند (برخلاف دایره هایی که فقط یک شعاع دارند)، منطقی است که یک مخزن تحت فشار استوانه ای بیضی دارای دو حداقل ضخامت (به جای تنها یک) باشد. آیا این درست است؟ اگر چنین است، چگونه می توان آنها را پیدا کرد؟
اگرچه یکسان نیستند، اما معمولاً میتوانند ناحیه موجود را در مقایسه با رگهای بیضوی (برای یک بعد معین A و B) بهینه کنند. به این ترتیب، اینها تقریباً همیشه انتخاب ترجیحی طراحی در مقایسه با بیضوی هستند و بیشتر به صورت تجاری در دسترس هستند. معادلات، در حالی که ناپیوستگی تنش غشایی را مدیریت می کنند، آسان تر هستند.
اساس فرض دیوار نازک
ما به راحتی می توانیم یک نسخه دیوار نازک از این را استخراج کنیم. می توان توجه داشت که بیضی نشان داده شده در بالا را می توان به صورت تمام نقاط بیان کرد
$(\frac{b}{2}\cos(\phi),\frac{a}{2}\sin(\phi))$
با پارامتر φ که از 0 تا $2\pi$ متغیر است. توجه داشته باشید که این همان زاویه از مرکز، θ نیست، اما با رابطه با این زاویه مرتبط است
$\tan(\theta) = \frac{b}{a} \tan(\phi)$
برای یک ϕ داده شده، تنش در یک ظرف جدار نازک به راحتی قابل مشاهده است. مشابه یک ظرف دایره ای، یک مقطع را به نقطه ای در ϕ مشخص تا مرکز می بریم. با استفاده از تقریب دیواره نازک مشابه مانند رگ های استوانه ای، فرض می کنیم تنش مماسی (غشاء) در سراسر این برش با ضخامت t یکنواخت است. ما فرض می کنیم که بدون توجه به ϕ به عنوان$t<<a ; t<<b$یکنواخت است. فاصله D(φ) تابعی است بر اساس ϕ از لبه، از طریق مرکز تا لبه دیگر به راحتی قابل انجام است.
$D(\phi) = \sqrt{b^2\cos^2(\phi) + a^2\sin^2(\phi)}$
. از آنجایی که دیوار به طور یکنواخت روی این برش با فشار P فشار داده می شود، پس واضح است که، مشابه دایره ها، برای بار در واحد طول بر اساس:
$PD(\phi) = 2t\sigma(\phi)$
$\sigma_t(\phi) = \frac{PD(\phi)}{2t}$.
با فرض ثابت بودن محیط
توجه داشته باشید که غلظت تنش قطعا ظاهر می شود، زیرا کشتی می خواهد شکل استوانه ای به خود بگیرد. با اجرای یک برش از هر دو محور x و y و اجرای یک تحلیل استاتیکی این بخش، متوجه میشویم که تنش مماسی بسیار کوچکتری از یک محور نسبت به دیگری ایجاد میشود. کرنش غیر یکنواخت مطمئناً باعث ایجاد گشتاورهای خمشی در مواد جدار نازک می شود.
بدون اجرای تجزیه و تحلیل دیواره ضخیم، این غلظت تنش را نمی توان دقیقاً تعیین کرد. برای این فرض دیوار نازک، ما به سادگی فرض می کنیم که محیط قبل و بعد از انحراف تقریباً یکسان می ماند. محیط یک بیضی با استفاده از انتگرال های بیضوی تعیین می شود. تعریف:
$k^2 = 1-\frac{a^2}{b^2}$
سپس محیط بیضی 2bE(k)$$ است، جایی که E انتگرال بیضی نوع دوم است. توجه می کنیم که k تابعی از b است. با گرفتن مشتق از این با توجه به b، و ریاضیات زیاد، به این نتیجه زیبا می رسیم که:$\frac{E(k)}{F(k)} = \frac{a^2}{b^2}$
ما E(k) و F(k)، انتگرال بیضوی نوع اول را به عنوان یک ثابت برای تغییرات کوچک در k ناشی از تغییرات a و b تقریب میکنیم. به این ترتیب، برای یک انقباض کوچک b، Δb، انبساط a، Δa را به صورت زیر مییابیم:
$\Delta a = - \frac{b^3}{a^3} \Delta b$
رابطه مکعبی نشان می دهد که بیضی های بسیار غیرعادی به سرعت از شکل بیضی به شکل استوانه ای تبدیل می شوند! به این ترتیب، تقریب های فوق به سرعت نامعتبر می شوند. منفی دلالت بر انبساط در مقابل انقباض است. با این اطلاعات، میتوان تلاش کرد تا غلظت تنش را به یک تقریب معقول حل کنیم. تنش "شعاعی" از نمای ایستا نشان می دهد که باید رشد شعاعی خطی داشته باشد، در حالی که تحلیل محیطی رشد شعاعی مکعبی را نشان می دهد. این انحراف خود را به عنوان یک نیرو نشان می دهد و غلظت خمشی را در نوک لبه b (بدترین حالت) تقریباً اضافه می کند:$M = \frac{Pb^2(b^2-a^2)}{4a^2}$
$\sigma_b = \frac{3Pb^2(b^2-a^2)}{2t^2a^2}$
این تنش باید b با محور دیگر جایگزین شود تا دو تنش حداکثر در رگ بدست آید. توجه داشته باشید که تنش مماسی اصلی باید به تنش خمشی اضافه شود. به این ترتیب، کل تنش در سمت محور طولانی خواهد بود:$\sigma_b = \frac{3Pb^2(b^2-a^2)}{2t^2a^2} + \frac{Pb}{2t}$
با جمع کردن تنش محوری تجزیه و تحلیل مورد به مورد خود (پیچیده است، اما می توان با تقسیم مساحت یک کلاهک بیضی بر محیط عجیب بیضی منطقی فرض کرد)، و تنش های یک Von- را دارید. استرس را از دست می دهد. این، به عنوان تابعی از ضخامت، روی حداکثر مقدار تنظیم می شود، و حداقل ضخامت نتیجه ای است که به تنش اجازه می دهد تا به حداکثر مقدار برسد. این بخش معمولاً در طراحی مخازن تحت فشار استفاده می شود، زیرا بارگذاری محیطی بیش از آنچه معادله شما فرض می کند، تنش می افزاید.$ \underbrace{-\nabla p - \rho\nabla \varphi = 0}_\textrm{equation of hydrostatics}\,.\tag{I}$
2 (مدول یانگ) چقرمگی = توانایی یک ماده برای جذب انرژی بدون شکست. در منحنی تنش-کرنش، ناحیه زیر منحنی اغلب معیاری برای چقرمگی در نظر گرفته می شود. در طرح زیر، ماده 2 چقرمگی بالاتری نسبت به ماده 1 دارد. (من باید آنها را به گونه ای طراحی می کردم که به وضوح متفاوت باشند، اما فرض کنید مساحت زیر منحنی ماده 2 بیشتر از مساحت زیر منحنی ماده 1 باشد.) بنابراین، ماده 2 ممکن است استحکام کمتری نسبت به ماده 1 داشته باشد اما می تواند انرژی کل بیشتری را قبل از شکست جذب کند.
سختی = توانایی یک ماده برای مقاومت در برابر تغییر شکل پلاستیک.
توجه داشته باشید که طرح دو منحنی ماده فرضی (خیالی) را منعکس می کند. بسیاری دیگر از پروفایل های منحنی تنش-کرنش امکان پذیر است. همچنین توجه داشته باشید که شرح چقرمگی ارائه شده در اینجا بر اساس چقرمگی مواد کلی است که تنها یک راه برای ارزیابی چقرمگی است. چقرمگی ضربه، چقرمگی بریدگی و چقرمگی شکست نیز وجود داره
ابتدا باید فشار دیوارها را محاسبه کنید. برای انجام این کار، یک صفحه برش را در هر قطری از ظرف تصور کنید. اکنون، نیروها را روی نیمی از کشتی متعادل کنید. در یک جهت، نیروی فشار سیال را دارید که مجموعاً به$F = \pi R^2 P$ می رسه. در جهت دیگر، تنها نیروی متعادل کننده، تنش در دیوارها است که بر روی سطح مقطع در معرض قرار می گیرند. نیرو در اینجا برابر است با $F = 2\pi R t \sigma_{wall}$، که t ضخامت دیوار است. با برابر قرار دادن این نیروها، می توانیم محاسبه کنیم که تنش در دیوار است
$\sigma_{wall} = \frac{P R}{2t}.$
حال به دلیل تقارن مسئله، و ساده سازی (معتبر) تنش ضخامت صفر، می توانیم حالت تنش کامل هر نقطه از دیوار را بنویسیم:
$\mathbf{\sigma} = \sigma_{wall}
\left(
\mathbf{e}_{\theta}
\otimes
\mathbf{e}_{\theta}
+
\mathbf{e}_{\phi}
\otimes
\mathbf{e}_{\phi}
\right)
+
0\;
(\mathbf{e}_{r}
\otimes
\mathbf{e}_{r})$
معیار بازده را بررسی کنم
برای محاسبه نقطه ای که تسلیم اتفاق می افتد، باید تنش کششی معادل میزس را محاسبه کنید. تعاریف معادل مختلفی وجود دارد، اما همه شما را به این نتیجه می رساند که برای جلوگیری از تغییر شکل پلاستیک، $\sigma_{wall} < \sigma_y$ که σy تنش تسلیم کششی تک محوری ماده است. بنابراین، حداکثر فشاری که ظرف می تواند قبل از تسلیم داشته باشد، است
$P < \frac{2\,t\,\sigma_{y}}{R}$
هنوز باید شکستگی را در نظر بگیرید، اما این یک بحث جداگانه است که بیشتر برای کلاس مهندسی مناسب است. (اگر این همان چیزی است که به دنبال آن هستید، می توانم به آنجا بروم...) با این معیار، معیار "نشتی قبل از شکست" وجود دارد که یک کران بالایی (غیر شهودی، اما بررسی می کند) روی ضخامت ایمن قرار می دهد. دیواره های رگ
نکته دیگری که باید در نظر داشت این است که فشار در مخزن با دما تغییر می کند. مطمئن شوید که این را در تجزیه و تحلیل خود با $PV = nRT$ یا یک معادله حالت مناسب دیگر در نظر بگیرید.
چگونه حداکثر فشاری که یک ظرف می تواند تحمل کند را محاسبه کنم؟در ابتدا، برای حل حداکثر فشاری که یک ظرف معین می تواند تحمل کند، فکر کردم که شاید بتوانم از مدول یانگ استفاده کنم، که تنش روی یک جسم را به فشاری که توسط یک جسم احساس می شود مرتبط می کند. تغییر در "طول" کره با در نظر گرفتن تغییر شعاع کره به مقدار کمی و دیدن اینکه چه اتفاقی برای یک عنصر کوچک افتاد (به هر حال این برنامه من بود) به دست میآورم. سپس متوجه شدم که از آنجایی که نیروی وارد شده به جسم واقعاً در جهت کشش نیست، بلکه عمود بر آن است
استحکام کششی نهایی وجود دارد! استحکام کششی نهایی بر حسب واحد فشار داده می شود، بنابراین فکر کردم که شاید پاسخ سوال من فقط عدد ذکر شده در مقاله ویکی پدیا باشد. این نه تنها به شدت رضایت بخش نبود، بلکه اشتباه به نظر می رسد، زیرا به نظر می رسد استحکام کششی نهایی دلالت بر این دارد که نیروی کشش در همان جهت کشش باشد. مدتی است که هیچ ایده خوبی به من نرسیده است، بنابراین فکر کردم باید بپرسم، چگونه حداکثر فشاری که یک ظرف معین می تواند داشته باشد را محاسبه کنم؟
مفهوم: استرس حلقه تنشی است که در طول محیط هنگام اعمال فشار ایجاد می شود. تنش حلقه عمود بر جهت محوری عمل می کند. تنش های حلقه ای کششی هستند و برای مقاومت در برابر اثر ترکیدن ناشی از اعمال فشار ایجاد می شوند.تنش در مخازن استوانهای
مطابق با شکل زیر مخزنی استوانهای را در نظر بگیرید. فرض کنید این مخزن حاوی گازی با فشار p است. مطابق با شکل زیر قطر و ضخامت این مخزن به ترتیب برابر با D و t و طول آن برابر با L در نظر گرفته شدهاند. برای بدست آوردن تنش مماسی، مخزن مطابق با شکل زیر برش زده میشود

پوسته آبی رنگ در تعادل است؛ بنابراین نیروی ناشی از فشارِ p با نیروی ناشی از تنش مماسی برابر است. در نتیجه با نوشتن رابطه تعادل داریم:
$\Large 2 T = F$
از طرفی نیروی T برابر با حاصل ضرب تنشِ σt در مساحتِ tL است. بنابراین رابطه فوق را میتوان به صورت زیر بازنویسی کرد.
$\Large 2 ( \sigma _ t t L ) = p D L$
نهایتا تنش مماسی در یک مخزن جدار نازکِ استوانهای با فشار p برابر با مقدار زیر بدست میآید.
$\Large 2 t \sigma _ t = p D$
رابطه ۱$\Large \boxed {\sigma_t = \dfrac { p D } { 2 t } }$
برای بدست آوردن تنش طولی کافی است تا مخزن استوانهای مطابق با شکل زیر، به صورت عمود به طول استوانه برش زده شود.
تنش در مخازن
نیروی وارد به انتهای استوانه برابر است با:$\Large F = p A = p \dfrac { \pi} {4} D ^2$
از طرفی تنش طولی تنها روی بخش جدار نازک اعمال میشود. مساحت این قسمت برابر با
$\large A = \pi D t$
است. از این رو نیروی ناشی از تنش طولی نیز برابر است با:
$\Large P _ T = \sigma _ L \pi D t$
در مرحله بعد معادله تعادل نیرویی را به صورت زیر بیان میکنیم.
$\Large \Sigma F _ H = 0$و$\Large P_T = F$و$\Large \sigma _ L \, \pi D t = p \dfrac {\pi} { 4 } D ^ 2$
نهایتا تنش طولی به صورت زیر بدست میآید.
$\Large \boxed {\sigma_t = \dfrac { p D } { 2 t } }$
توجه داشته باشید در روابط فوق منظور از فشار، در حقیقت اختلاف فشار داخل و بیرونِ مخزن است. بنابراین با فرض این که فشار داخلی برابر با pi و فشار خارجی برابر با po باشد، رابطه زیر را میتوان برای تنش طولی بیان کرد.$\Large F = p A = p \dfrac { \pi} {4} D ^2$
با توجه به روابط ۱ و ۲، رابطه زیر را میتوان بین تنشهای افقی و عمودی نوشت.
$\Large \sigma _ t = 2 \sigma _ L$
تنش در مخازن کروی
به دلیل متقارن بودن شکل کره نسبت به تمامی محورهایی که از مرکز آن عبور میکنند، تنش در پوسته یک مخزن کروی، در تمامی جهات با هم برابر هستند. از این رو به منظور محاسبه تنش، تنها کافی است تا مطابق با شکل زیر، کره را در جهتی دلخواه برش بزنید.
تنش در مخازن
نیروی داخلیِ ناشی از فشار که به نیمکره وارد میشود، برابر است با:
$\Large P = p ( \frac { 1 } { 4 } \pi D ^ 2 )$
این نیرو برابر با تنشی است که به جداره وارد میشود. بنابراین میتوان گفت:
$\Large P_T = F$
$\Large \sigma \pi D t = p (\frac {1}{4} \pi D ^ 2)$
نهایتا تنش در جداره یک مخزن کروی با فشار p برابر است با:
$\Large \boxed { \sigma = \dfrac { p D } { 4 t } }$
نحوه محاسبه مقاومت فشار خارجی سیلندرها و کره ها
اگر دیواره های مخزن به اندازه کافی نازک باشد، تحت فشار خارجی نه به دلیل رسیدن مواد به نقطه تسلیم، بلکه به دلیل ناپایداری (کمانش) از بین می رود. به عنوان مثال، یک فشار بحرانی برای یک استوانه بی نهایت جدار نازک با شکل کامل $p=\frac{2 E}{1-\mu^2}(t/D)^3$ است، که در آن E مدول الاستیسیته، μ نسبت پواسون، t ضخامت دیواره و D قطر سیلندر است
حداقل ضخامت یک مخزن تحت فشار سیلندر بیضویبرای مخازن تحت فشار به شکل استوانههای دایرهای، میتوانیم از σhoop=prt استفاده کنیم تا حداقل ضخامت پوست را با تنظیم تنش حلقه حداکثر مقدار مجاز و سپس حل کردن t استفاده کنیم. اما، سیلندرهای بیضوی (پیچیده تر) چطور؟
از آنجایی که بیضی ها دارای یک محور نیمه اصلی و یک محور نیمه فرعی هستند (برخلاف دایره هایی که فقط یک شعاع دارند)، منطقی است که یک مخزن تحت فشار استوانه ای بیضی دارای دو حداقل ضخامت (به جای تنها یک) باشد. آیا این درست است؟ اگر چنین است، چگونه می توان آنها را پیدا کرد؟
اگرچه یکسان نیستند، اما معمولاً میتوانند ناحیه موجود را در مقایسه با رگهای بیضوی (برای یک بعد معین A و B) بهینه کنند. به این ترتیب، اینها تقریباً همیشه انتخاب ترجیحی طراحی در مقایسه با بیضوی هستند و بیشتر به صورت تجاری در دسترس هستند. معادلات، در حالی که ناپیوستگی تنش غشایی را مدیریت می کنند، آسان تر هستند.
اساس فرض دیوار نازک
ما به راحتی می توانیم یک نسخه دیوار نازک از این را استخراج کنیم. می توان توجه داشت که بیضی نشان داده شده در بالا را می توان به صورت تمام نقاط بیان کرد
$(\frac{b}{2}\cos(\phi),\frac{a}{2}\sin(\phi))$
با پارامتر φ که از 0 تا $2\pi$ متغیر است. توجه داشته باشید که این همان زاویه از مرکز، θ نیست، اما با رابطه با این زاویه مرتبط است
$\tan(\theta) = \frac{b}{a} \tan(\phi)$
برای یک ϕ داده شده، تنش در یک ظرف جدار نازک به راحتی قابل مشاهده است. مشابه یک ظرف دایره ای، یک مقطع را به نقطه ای در ϕ مشخص تا مرکز می بریم. با استفاده از تقریب دیواره نازک مشابه مانند رگ های استوانه ای، فرض می کنیم تنش مماسی (غشاء) در سراسر این برش با ضخامت t یکنواخت است. ما فرض می کنیم که بدون توجه به ϕ به عنوان$t<<a ; t<<b$یکنواخت است. فاصله D(φ) تابعی است بر اساس ϕ از لبه، از طریق مرکز تا لبه دیگر به راحتی قابل انجام است.
$D(\phi) = \sqrt{b^2\cos^2(\phi) + a^2\sin^2(\phi)}$
. از آنجایی که دیوار به طور یکنواخت روی این برش با فشار P فشار داده می شود، پس واضح است که، مشابه دایره ها، برای بار در واحد طول بر اساس:
$PD(\phi) = 2t\sigma(\phi)$
$\sigma_t(\phi) = \frac{PD(\phi)}{2t}$.
با فرض ثابت بودن محیط
توجه داشته باشید که غلظت تنش قطعا ظاهر می شود، زیرا کشتی می خواهد شکل استوانه ای به خود بگیرد. با اجرای یک برش از هر دو محور x و y و اجرای یک تحلیل استاتیکی این بخش، متوجه میشویم که تنش مماسی بسیار کوچکتری از یک محور نسبت به دیگری ایجاد میشود. کرنش غیر یکنواخت مطمئناً باعث ایجاد گشتاورهای خمشی در مواد جدار نازک می شود.
بدون اجرای تجزیه و تحلیل دیواره ضخیم، این غلظت تنش را نمی توان دقیقاً تعیین کرد. برای این فرض دیوار نازک، ما به سادگی فرض می کنیم که محیط قبل و بعد از انحراف تقریباً یکسان می ماند. محیط یک بیضی با استفاده از انتگرال های بیضوی تعیین می شود. تعریف:
$k^2 = 1-\frac{a^2}{b^2}$
سپس محیط بیضی 2bE(k)$$ است، جایی که E انتگرال بیضی نوع دوم است. توجه می کنیم که k تابعی از b است. با گرفتن مشتق از این با توجه به b، و ریاضیات زیاد، به این نتیجه زیبا می رسیم که:$\frac{E(k)}{F(k)} = \frac{a^2}{b^2}$
ما E(k) و F(k)، انتگرال بیضوی نوع اول را به عنوان یک ثابت برای تغییرات کوچک در k ناشی از تغییرات a و b تقریب میکنیم. به این ترتیب، برای یک انقباض کوچک b، Δb، انبساط a، Δa را به صورت زیر مییابیم:
$\Delta a = - \frac{b^3}{a^3} \Delta b$
رابطه مکعبی نشان می دهد که بیضی های بسیار غیرعادی به سرعت از شکل بیضی به شکل استوانه ای تبدیل می شوند! به این ترتیب، تقریب های فوق به سرعت نامعتبر می شوند. منفی دلالت بر انبساط در مقابل انقباض است. با این اطلاعات، میتوان تلاش کرد تا غلظت تنش را به یک تقریب معقول حل کنیم. تنش "شعاعی" از نمای ایستا نشان می دهد که باید رشد شعاعی خطی داشته باشد، در حالی که تحلیل محیطی رشد شعاعی مکعبی را نشان می دهد. این انحراف خود را به عنوان یک نیرو نشان می دهد و غلظت خمشی را در نوک لبه b (بدترین حالت) تقریباً اضافه می کند:$M = \frac{Pb^2(b^2-a^2)}{4a^2}$
$\sigma_b = \frac{3Pb^2(b^2-a^2)}{2t^2a^2}$
این تنش باید b با محور دیگر جایگزین شود تا دو تنش حداکثر در رگ بدست آید. توجه داشته باشید که تنش مماسی اصلی باید به تنش خمشی اضافه شود. به این ترتیب، کل تنش در سمت محور طولانی خواهد بود:$\sigma_b = \frac{3Pb^2(b^2-a^2)}{2t^2a^2} + \frac{Pb}{2t}$
با جمع کردن تنش محوری تجزیه و تحلیل مورد به مورد خود (پیچیده است، اما می توان با تقسیم مساحت یک کلاهک بیضی بر محیط عجیب بیضی منطقی فرض کرد)، و تنش های یک Von- را دارید. استرس را از دست می دهد. این، به عنوان تابعی از ضخامت، روی حداکثر مقدار تنظیم می شود، و حداقل ضخامت نتیجه ای است که به تنش اجازه می دهد تا به حداکثر مقدار برسد. این بخش معمولاً در طراحی مخازن تحت فشار استفاده می شود، زیرا بارگذاری محیطی بیش از آنچه معادله شما فرض می کند، تنش می افزاید.$ \underbrace{-\nabla p - \rho\nabla \varphi = 0}_\textrm{equation of hydrostatics}\,.\tag{I}$

-
sohrab 4242
نام: سهراب نعمتی
عضویت : سهشنبه ۱۴۰۱/۹/۸ - ۲۱:۴۷
پست: 11-
- جنسیت:
Re: الکترولیز آب تحت فشار
سلام ضمن تشکر از استاد محترم که جواب سوالات مرا دادند من یک محقق در مورد انرژیهای نو هستم اگر امکان باشه میخواستم با شما بیشتر آشنا شوم و سطح مطالعاتی شما را بدانم
-
sohrab 4242
نام: سهراب نعمتی
عضویت : سهشنبه ۱۴۰۱/۹/۸ - ۲۱:۴۷
پست: 11-
- جنسیت:
Re: الکترولیز آب تحت فشار
سلام استاد حداکثر فشاری که میتوان از طریق الکترولیز و انباشته شدن گازها بدست اورد چقدر است؟ ممنون
- rohamavation
نام: roham hesami radرهام حسامی راد
محل اقامت: 100 مایلی شمال لندن جاده آیلستون، لستر، لسترشر. LE2
عضویت : سهشنبه ۱۳۹۹/۸/۲۰ - ۰۸:۳۴
پست: 3286-
سپاس: 5494
- جنسیت:
تماس:
Re: الکترولیز آب تحت فشار
ببین من قبلش هم گفتم بهتون حداکثر فشار گازی که می توانید در ولتامتر هافمن انتظار داشته باشید فشار اتمسفر به اضافه فشار ستون آب در سیلندر میانی (1 atm/10m) است.
پس برای یک دستگاه با اندازه معقول شما به شرایطی نمیرسین که مجبور بشین اثرات فشار برگشتی را در نظر بگیرین که ممکنه تولید هیدروژن یا اکسیژن را متوقف کنه
با توجه به اینکه سطح مقطع هر سه سیلندر یکسانه فشار هیدروژن کمی بیشتر از فشار اکسیژنه زیرا ستون آبی که فشار را اضافه می کنه بیشتر است
خوب الکترولیز قلیایی یک فناوری الکترولیز آب هست -.الکترولیز فشار بالا (HPE) الکترولیز آب با تجزیه آب (H2O) به اکسیژن (O2) و گاز هیدروژن (H2) به دلیل عبور جریان الکتریکی از ابه .اینم تو هوافضا کاربرد داره ایستگاه International Space Station ، خروجی هیدروژن فشرده در حدود 12-20 مگا پاسکال (120-200 بار) در 70 درجه سانتی گراد است با تحت فشار قرار دادن هیدروژن در الکترولیز نیاز به یک کمپرسور هیدروژن خارجی حذف میشه میانگین مصرف انرژی برای فشرده سازی فشار دیفرانسیل داخلی خیلی کمه چون که قدرت تراکم مورد نیاز برای آب کمتر از هیدروژن-گازه آب تا فشار بالا پمپ میشه در رویکرد دیگر از فشار دیفرانسیل استفاده میشه
الکترولیز فشار فوقالعاده، الکترولیز فشار بالا است که در 340-690 بار (5000-10000 psi) کار میکنه
برای هر گاز حداکثر ضریب تراکم پذیری (Q) وجود داره. و از آنجایی که ما دو محصول هیدروژن و اکسیژن داریم کمترین (Q) که برای اکسیژن است پیش میرویم بنابراین در صورت الکترولیز آب تحت فشار بالا انتظار داریم واکنش ماا با رسیدن فشار داخل (Q) متوقف بشه اکنون برای پیدا کردن (Q). چگونه این کار را انجام دهیم؟ برای یک گاز باید ببینید چگالی آن در حالت مایع چقدر است (به عنوان مثال لیتر در کیلوگرم) سپس باید حداکثر چگالی باشد که می توانید با هر فشاری به دست آورید زیرا پس از آن فشار باعث ایجاد اتم ها می شود.یک محیط پرفشار تمایل داره مایعات را بر گازها ترجیح بده، تا جایی که مایعات چگالی بالاتری دارند. بنابراین هر چه فشار بیشتر باشه، ولتاژ بیشتری باید اعمال کنید تا واکنش H2O --> H2+O2 انجام بشه
اما، با ولتاژ به اندازه کافی بالا، همیشه باید امکان پذیر باشد. اگر ولتاژ را به اندازه کافی بالا ببرید، در نهایت هر واکنش الکترولیتی رخ خواهد داد. الکترولیز فقط در صورتی غیرممکن می شود (در عمل) (در هر ولتاژی غیرممکنه . من مطمئن نیستم که واکنش های رقابتی برای الکترولیز آب خالص در یک محیط پرفشار چیه . به عنوان مثال، احتمالاً H2O --> H2 + O3 (گاز ازن) در فشار کافی بالا بر H2O --> H2 + O2 ترجیح داده می شود.معادله واندروالس ایزوترم یک گاز را با توجه به فشار و حجم توصیف می کنه. اولین ریشه واندروالس (اولین راه حل معادله مکعب) نقطه شبنم را به شما میده که نقطه ای است که اولین قطره مایع از گاز تشکیل میشه ریشه دیگر معادله به اصطلاح نقطه حبابه ، زمانی است که اولین قطره مایع ترکیب تشکیل می شه. ریشه میانی همیشه در منطقه ای یافت می شود که مایع و بخار با هم وجود داشته باشه اما همانطور که یک منطقه است و نه یک نقطه، خود آن ریشه نیز معنای فیزیکی ندارد.$V_m^3-\dfrac{RT+bP}{P}V_m^2+\dfrac{a}{P}V_m-\dfrac{ab}{P}=0$
هنگامی که فشار را به عنوان مثال افزایش می دهید. بخار آبی، شما میرسید تا آب و آب جامد داشته باشید. به طور مشابه وقتی فشار اکسیژن را افزایش می دهید، اکسیژن مایع و اکسیژن جامد دریافت می کنید، اما زمانی که شما در دمای بحرانی قرار دارید (که برای اکسیژن 118.6- درجه سانتی گراد است) معتبر است. هنگامی که شما بالاتر از دمای بحرانی هستین، تنها وضعیتی از اکسیژن گاز مایع وجود دارد که صرف نظر از فشار در همان فازه /حالا بازم من نفهمیدم ببین اگه محاسبات باشه که با ولتاژ اعمالی و رابطه با فشار که خیلی پیچیده و منم فرمول نمیدونم دوستام هم نمیدونن .ولا به درسم هم ربطی نداره از استادهایم بپرسم رشته و تخصصون چیز دیگه هست دینامیک و ترمودینامیک و ایرو و اینا کلا چیز دیگه هست .فقط استادهای شیمی و بچه های ارشد شیمی میتونن کمک کنن .بازم براتون میپرسم.
پس برای یک دستگاه با اندازه معقول شما به شرایطی نمیرسین که مجبور بشین اثرات فشار برگشتی را در نظر بگیرین که ممکنه تولید هیدروژن یا اکسیژن را متوقف کنه
با توجه به اینکه سطح مقطع هر سه سیلندر یکسانه فشار هیدروژن کمی بیشتر از فشار اکسیژنه زیرا ستون آبی که فشار را اضافه می کنه بیشتر است
خوب الکترولیز قلیایی یک فناوری الکترولیز آب هست -.الکترولیز فشار بالا (HPE) الکترولیز آب با تجزیه آب (H2O) به اکسیژن (O2) و گاز هیدروژن (H2) به دلیل عبور جریان الکتریکی از ابه .اینم تو هوافضا کاربرد داره ایستگاه International Space Station ، خروجی هیدروژن فشرده در حدود 12-20 مگا پاسکال (120-200 بار) در 70 درجه سانتی گراد است با تحت فشار قرار دادن هیدروژن در الکترولیز نیاز به یک کمپرسور هیدروژن خارجی حذف میشه میانگین مصرف انرژی برای فشرده سازی فشار دیفرانسیل داخلی خیلی کمه چون که قدرت تراکم مورد نیاز برای آب کمتر از هیدروژن-گازه آب تا فشار بالا پمپ میشه در رویکرد دیگر از فشار دیفرانسیل استفاده میشه
الکترولیز فشار فوقالعاده، الکترولیز فشار بالا است که در 340-690 بار (5000-10000 psi) کار میکنه
برای هر گاز حداکثر ضریب تراکم پذیری (Q) وجود داره. و از آنجایی که ما دو محصول هیدروژن و اکسیژن داریم کمترین (Q) که برای اکسیژن است پیش میرویم بنابراین در صورت الکترولیز آب تحت فشار بالا انتظار داریم واکنش ماا با رسیدن فشار داخل (Q) متوقف بشه اکنون برای پیدا کردن (Q). چگونه این کار را انجام دهیم؟ برای یک گاز باید ببینید چگالی آن در حالت مایع چقدر است (به عنوان مثال لیتر در کیلوگرم) سپس باید حداکثر چگالی باشد که می توانید با هر فشاری به دست آورید زیرا پس از آن فشار باعث ایجاد اتم ها می شود.یک محیط پرفشار تمایل داره مایعات را بر گازها ترجیح بده، تا جایی که مایعات چگالی بالاتری دارند. بنابراین هر چه فشار بیشتر باشه، ولتاژ بیشتری باید اعمال کنید تا واکنش H2O --> H2+O2 انجام بشه
اما، با ولتاژ به اندازه کافی بالا، همیشه باید امکان پذیر باشد. اگر ولتاژ را به اندازه کافی بالا ببرید، در نهایت هر واکنش الکترولیتی رخ خواهد داد. الکترولیز فقط در صورتی غیرممکن می شود (در عمل) (در هر ولتاژی غیرممکنه . من مطمئن نیستم که واکنش های رقابتی برای الکترولیز آب خالص در یک محیط پرفشار چیه . به عنوان مثال، احتمالاً H2O --> H2 + O3 (گاز ازن) در فشار کافی بالا بر H2O --> H2 + O2 ترجیح داده می شود.معادله واندروالس ایزوترم یک گاز را با توجه به فشار و حجم توصیف می کنه. اولین ریشه واندروالس (اولین راه حل معادله مکعب) نقطه شبنم را به شما میده که نقطه ای است که اولین قطره مایع از گاز تشکیل میشه ریشه دیگر معادله به اصطلاح نقطه حبابه ، زمانی است که اولین قطره مایع ترکیب تشکیل می شه. ریشه میانی همیشه در منطقه ای یافت می شود که مایع و بخار با هم وجود داشته باشه اما همانطور که یک منطقه است و نه یک نقطه، خود آن ریشه نیز معنای فیزیکی ندارد.$V_m^3-\dfrac{RT+bP}{P}V_m^2+\dfrac{a}{P}V_m-\dfrac{ab}{P}=0$
هنگامی که فشار را به عنوان مثال افزایش می دهید. بخار آبی، شما میرسید تا آب و آب جامد داشته باشید. به طور مشابه وقتی فشار اکسیژن را افزایش می دهید، اکسیژن مایع و اکسیژن جامد دریافت می کنید، اما زمانی که شما در دمای بحرانی قرار دارید (که برای اکسیژن 118.6- درجه سانتی گراد است) معتبر است. هنگامی که شما بالاتر از دمای بحرانی هستین، تنها وضعیتی از اکسیژن گاز مایع وجود دارد که صرف نظر از فشار در همان فازه /حالا بازم من نفهمیدم ببین اگه محاسبات باشه که با ولتاژ اعمالی و رابطه با فشار که خیلی پیچیده و منم فرمول نمیدونم دوستام هم نمیدونن .ولا به درسم هم ربطی نداره از استادهایم بپرسم رشته و تخصصون چیز دیگه هست دینامیک و ترمودینامیک و ایرو و اینا کلا چیز دیگه هست .فقط استادهای شیمی و بچه های ارشد شیمی میتونن کمک کنن .بازم براتون میپرسم.


