راه حل پارادوکس گیبس چیست؟
ارسال شده: دوشنبه ۱۴۰۰/۱۰/۲۷ - ۰۷:۴۵
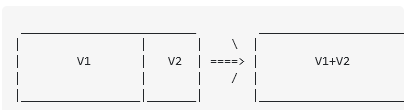
من مقداری گاز از ذرات یکسان دارم و آنها در جعبه ای هستند که توسط یک تقسیم کننده قابل جابجایی به دو قسمت تقسیم شده است. حال سوال این است که "اگر من تقسیم کننده را حذف کنم، چرا باید تغییر در آنتروپی 0 باشد؟" پاسخ استاندارد در سوال مرتبط با بالا داده شده است. ایده اصلی پاسخ این است که قرار است ذرات غیر قابل تشخیص در نظر گرفته شوند. اگر با ذرات به این شکل رفتار کنید، متوجه می شوید که با حذف پارتیشن، تغییری در آنتروپی ایجاد نمی شود.
من این پاسخ را درک میکنم، و فکر میکنم باید برای اتمهای یکسان کار کند، اما شما به راحتی میتوانید موقعیتی را تصور کنید که در آن مجموعهای از اجسام قابل تشخیص دارید، مثلاً برخی از نانوذرات با تعداد اتمهای سازنده متفاوت.
علاوه بر این، شما باید بتوانید گازی از ذرات یکسان را به عنوان اجسام قابل تشخیص کلاسیک در نظر بگیرید، و همچنان پاسخ درست را از مکانیک آماری دریافت کنید. می توانم بگویم این یک بررسی خوب برای درک مکانیک آماری است.
اگر این انگیزه کافی برای دستیابی به تفکیک پذیری متناوب برای پارادوکس نیست، این پارادوکس را در نظر بگیرید، که اساساً به همان وضوحی نیاز دارد که پارادوکس گیبس دارد: دو سیستم را در ابتدا در تماس حرارتی و در تعادل حرارتی تصور کنید. حالا فرض کنید از هم جدا شده اند. در اینجا ممکن است فکر کنیم که آنتروپی در این فرآیند کاهش مییابد زیرا در پیکربندی اولیه انرژی هر دو سیستم تا زمانی که مجموع آنها ثابت میماند تغییر میکند. پس از جداسازی، انرژی سیستم ها در مقداری ثابت می شود. واضح است که مجموعه حالت های نهایی زیر مجموعه ای از حالت های اولیه است، بنابراین آنتروپی کاهش یافته است. این قیاس پارادوکس گیبس است که در آن به جای اینکه سیستمها عدد ذرات را مبادله کنند، در حال تبادل انرژی هستند. من انتظار دارم که اساساً همان وضوح را داشته باشد.
بنابراین سوال من این است، "چرا باید تغییر در آنتروپی صفر باشد، حتی در ذرات قابل تشخیص؟
بنابراین سوال من این است که "چرا باید تغییر در آنتروپی صفر باشد، حتی اگر ذرات قابل تشخیص باشند؟"
در فیزیک آماری، آنتروپی را می توان به روش های مختلفی تعریف کرد.
با توجه به محدودیت های ماکروسکوپی (حجم) یک امکان این است که آن را به عنوان گزارش فضای فاز قابل دسترسی تعریف کنیم. چنین آنتروپی تابعی همگن از انرژی، حجم و تعداد ذرات نیست. اگر دیوار برداشته شود،
راه دیگر این است که آن را به عنوان لاگ فضای فاز قابل دسترسی تقسیم بر تعداد جایگشت ذرات تعریف کنیم. این آنتروپی تابعی همگن از انرژی، حجم و تعداد ذرات است. اگر دیوار برداشته شود، این آنتروپی ثابت می ماند.
هر دوی این تعاریف معتبر هستند و به مفاهیم مختلفی از آنتروپی منجر می شوند. آنتروپی "درست" وجود ندارد. با این حال، برای راحتی، اغلب ترجیح داده می شود از تعریف دوم استفاده شود. سپس آنتروپی دو زیرسیستم متقابل در حالت تعادل، مجموع آنتروپیهای متناظر آنها است و حذف دیواره آنتروپی را تغییر نمیدهد، که قراردادهای بسیار عملی هستند که قبلاً از ترمودینامیک کلاسیک انتظار میرفتند.ذرات کلاسیک یکسان قابل تشخیص هستند. این تمایز بر تعداد راههایی که W یک کلان حالت میتواند در سطح میکرو تحقق یابد تأثیر میگذارد، و از رابطه$ S = k ln W$ منجر به بیان غیر گسترده برای آنتروپی میشود. این نتیجه معمولاً به دلیل ناهماهنگی آن با ترمودینامیک نادرست در نظر گرفته می شود. تغییر آنتروپی باید صفر باشد - و اساساً صفر است، در نظریه درستی که عدم تمایز را در نظر می گیرد - زیرا غشای نازک به طور مادی سیستم را تغییر نمی دهد و یک آنتروپی کوچک به خودی خود حمل می کند. دلیل اول کافی است: حذف غشا یک فرآیند برگشت پذیر است - ممکن است غشاء را دوباره اضافه کنید - بنابراین آنتروپی باید صفر باشد. آنتروپی نمیتواند در طول یک فرآیند برگشتپذیر افزایش یابد، زیرا با معکوس شدن فرآیند کاهش مییابد - و این قانون دوم ترمودینامیک را نقض میکند.به عبارت دیگر، برگشت پذیری بدیهی غشای غیرفیزیکی به این معنی است که $\delta S = \delta Q/T$ که در آن δQ گرمای جریان یافته به سیستم است – اما به وضوح صفر است..I hope I help you understand the question. Roham Hesami

 رهام حسامی ترم پنجم مهندسی هوافضا
رهام حسامی ترم پنجم مهندسی هوافضا
من این پاسخ را درک میکنم، و فکر میکنم باید برای اتمهای یکسان کار کند، اما شما به راحتی میتوانید موقعیتی را تصور کنید که در آن مجموعهای از اجسام قابل تشخیص دارید، مثلاً برخی از نانوذرات با تعداد اتمهای سازنده متفاوت.
علاوه بر این، شما باید بتوانید گازی از ذرات یکسان را به عنوان اجسام قابل تشخیص کلاسیک در نظر بگیرید، و همچنان پاسخ درست را از مکانیک آماری دریافت کنید. می توانم بگویم این یک بررسی خوب برای درک مکانیک آماری است.
اگر این انگیزه کافی برای دستیابی به تفکیک پذیری متناوب برای پارادوکس نیست، این پارادوکس را در نظر بگیرید، که اساساً به همان وضوحی نیاز دارد که پارادوکس گیبس دارد: دو سیستم را در ابتدا در تماس حرارتی و در تعادل حرارتی تصور کنید. حالا فرض کنید از هم جدا شده اند. در اینجا ممکن است فکر کنیم که آنتروپی در این فرآیند کاهش مییابد زیرا در پیکربندی اولیه انرژی هر دو سیستم تا زمانی که مجموع آنها ثابت میماند تغییر میکند. پس از جداسازی، انرژی سیستم ها در مقداری ثابت می شود. واضح است که مجموعه حالت های نهایی زیر مجموعه ای از حالت های اولیه است، بنابراین آنتروپی کاهش یافته است. این قیاس پارادوکس گیبس است که در آن به جای اینکه سیستمها عدد ذرات را مبادله کنند، در حال تبادل انرژی هستند. من انتظار دارم که اساساً همان وضوح را داشته باشد.
بنابراین سوال من این است، "چرا باید تغییر در آنتروپی صفر باشد، حتی در ذرات قابل تشخیص؟
بنابراین سوال من این است که "چرا باید تغییر در آنتروپی صفر باشد، حتی اگر ذرات قابل تشخیص باشند؟"
در فیزیک آماری، آنتروپی را می توان به روش های مختلفی تعریف کرد.
با توجه به محدودیت های ماکروسکوپی (حجم) یک امکان این است که آن را به عنوان گزارش فضای فاز قابل دسترسی تعریف کنیم. چنین آنتروپی تابعی همگن از انرژی، حجم و تعداد ذرات نیست. اگر دیوار برداشته شود،
راه دیگر این است که آن را به عنوان لاگ فضای فاز قابل دسترسی تقسیم بر تعداد جایگشت ذرات تعریف کنیم. این آنتروپی تابعی همگن از انرژی، حجم و تعداد ذرات است. اگر دیوار برداشته شود، این آنتروپی ثابت می ماند.
هر دوی این تعاریف معتبر هستند و به مفاهیم مختلفی از آنتروپی منجر می شوند. آنتروپی "درست" وجود ندارد. با این حال، برای راحتی، اغلب ترجیح داده می شود از تعریف دوم استفاده شود. سپس آنتروپی دو زیرسیستم متقابل در حالت تعادل، مجموع آنتروپیهای متناظر آنها است و حذف دیواره آنتروپی را تغییر نمیدهد، که قراردادهای بسیار عملی هستند که قبلاً از ترمودینامیک کلاسیک انتظار میرفتند.ذرات کلاسیک یکسان قابل تشخیص هستند. این تمایز بر تعداد راههایی که W یک کلان حالت میتواند در سطح میکرو تحقق یابد تأثیر میگذارد، و از رابطه$ S = k ln W$ منجر به بیان غیر گسترده برای آنتروپی میشود. این نتیجه معمولاً به دلیل ناهماهنگی آن با ترمودینامیک نادرست در نظر گرفته می شود. تغییر آنتروپی باید صفر باشد - و اساساً صفر است، در نظریه درستی که عدم تمایز را در نظر می گیرد - زیرا غشای نازک به طور مادی سیستم را تغییر نمی دهد و یک آنتروپی کوچک به خودی خود حمل می کند. دلیل اول کافی است: حذف غشا یک فرآیند برگشت پذیر است - ممکن است غشاء را دوباره اضافه کنید - بنابراین آنتروپی باید صفر باشد. آنتروپی نمیتواند در طول یک فرآیند برگشتپذیر افزایش یابد، زیرا با معکوس شدن فرآیند کاهش مییابد - و این قانون دوم ترمودینامیک را نقض میکند.به عبارت دیگر، برگشت پذیری بدیهی غشای غیرفیزیکی به این معنی است که $\delta S = \delta Q/T$ که در آن δQ گرمای جریان یافته به سیستم است – اما به وضوح صفر است..I hope I help you understand the question. Roham Hesami